
扫码关注公众号
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
益方生物
688382 |
-4.53%
|
最新:19.6
开盘:20.17 昨收:20.53 |
开盘%:-1.75%
振幅%:7.21% 换手%:4.01% |
最高:20.63
最低:19.15 量比:1.16 |
总市值:113 亿
流通值:79 亿 成交额:4 亿 |
- 基本信息
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- Deepseek分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
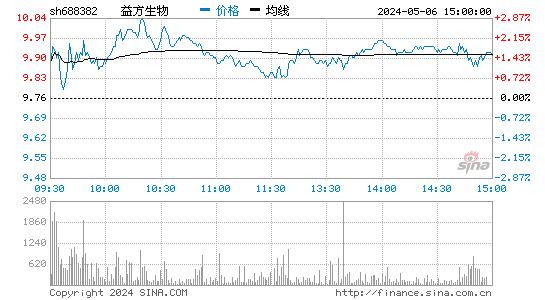
- 分时图
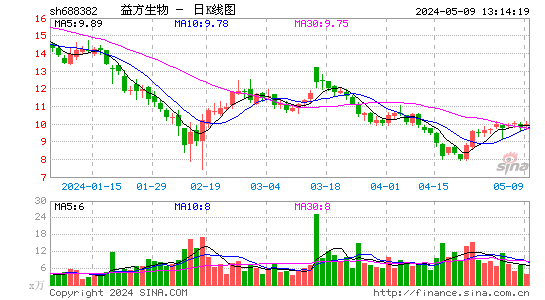
- 日K图
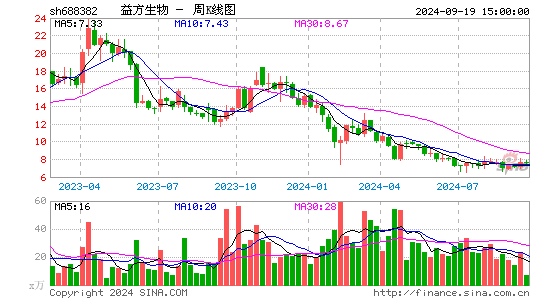
- 周K图
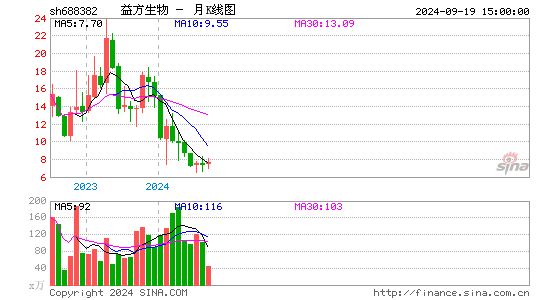
- 月K图
益方生物-U股票详解
创新型药物研发企业的股市表现与业务概览
一、益方生物-U股市概况
益方生物-U(股票代码:688382)作为科创板上市公司,其股价和市值随市场波动而不断变化。截至最新数据,益方生物-U的总市值约为74.40亿元,市盈率TTM为21.39。近期,该股票受到市场关注,融资净买入情况良好。
二、公司业务与产品
业务领域:益方生物-U聚焦于肿瘤、代谢性疾病等重大疾病领域,致力于研制具有自主知识产权的创新药物。
主要产品:公司主要产品包括甲磺酸贝福替尼(BPID0316)、D-1553、D-0502等多个在研药物,涵盖了激酶抑制剂、蛋白抑制剂等多种类型。
三、研发实力与合作
益方生物-U拥有强大的研发实力,持续投入高额研发费用,以推动药物的研发进程。同时,公司与多家知名企业及研究机构开展合作,共同推进创新药物的研发。
四、市场前景与挑战
随着全球对创新药物需求的不断增长,益方生物-U面临广阔的市场前景。然而,药物研发过程中的技术风险、市场竞争以及政策变化等因素都可能对公司的未来发展产生影响。
总结
益方生物-U作为一家创新型药物研发企业,拥有强大的研发实力和丰富的产品线,市场前景广阔。然而,投资者也需关注其面临的市场竞争和技术风险等因素。关键词:益方生物-U, 创新型药物研发, 肿瘤药物, 代谢性疾病药物, 市场前景。
2025-04-02 19:52
益方生物:ABA-Bio拟减持不超过1.6%
2025-03-10 07:52
【益方生物:D-2570治疗银屑病II期临床研究结果在2025年美国皮肤病学会(AAD)年会发布】益方生物公告,2025年3月8日,公司自主研发的 TYK2 抑制剂 D-2570 治疗中重度斑块状银屑病的 II 期临床研究结果,以口头报告形式在 2025 年美国皮肤病学会(AAD)年会的最新突破研究摘要(Late-Breaking Abstracts)部分发布。II 期临床研究数据显示,D-2570 治疗中重度银屑病患者的疗效显著优于安慰剂,也优于目前已上市的同类 TYK2 抑制剂,在效果上也可与抗体生物药(如抗 IL-17A,抗 IL-23 抗体)相媲美,总体耐受性良好,未来有望为包括银屑病在内的自身免疫性疾病患者提供一种新的治疗选择。
2025-01-06 18:22
【益方生物:美国新泽西地区法院驳回美国倍而达对公司的诉讼请求】1月6日电,益方生物公告,公司收到美国新泽西地区法院书面裁定,就美国倍而达对公司、Yueheng Jiang (江岳恒)、Wansheng Jerry Liu和Fox Rothschild, LLP提起的民事诉讼事项,法院裁定驳回原告诉讼请求。裁定驳回了原告第一项诉讼请求(即违反联邦《保护商业秘密法》项下的商业秘密盗窃)且原告对同一事由不得再次提起诉讼。此外,基于其余诉讼请求不属于联邦法院管辖,本案件被驳回。原告可在30日内向州法院提起诉讼。本次诉讼不会对公司损益产生负面影响。但鉴于原告可在判决后一定期限内向州法院提起诉讼,公司将密切关注案件后续情况并及时履行信息披露义务。
2024-12-24 19:13
益方生物:股东LAV Apex、LAV Alpha、LAV Inventis、苏州礼康拟减持不超过2.8%。
2024-12-03 16:22
益方生物:自主研发的靶向TYK2的新型口服选择性抑制剂D-2570已于近日完成针对银屑病的II期临床试验,并取得了积极的临床试验结果
2024-11-11 08:22
【益方生物:格索雷塞片获批上市】益方生物公告,近日,公司与正大天晴药业集团股份有限公司合作开发的1类创新药格索雷塞片(商品名称:安方宁)获得国家药品监督管理局批准上市,该药适用于治疗至少接受过一种系统性治疗的鼠类肉瘤病毒癌基因(KRAS)G12C突变型的晚期非小细胞肺癌(NSCLC)成人患者。
2024-09-29 17:27
【益方生物:一审判决驳回原告米拉蒂公司全部诉讼请求】益方生物公告,公司及全资子公司美国益方、公司董事XING DAI(代星)因被诉侵害米拉蒂公司和亚雷公司技术秘密案,收到上海知识产权法院的《民事判决书》。法院一审判决驳回原告全部诉讼请求。涉案金额为9,900万元。本次诉讼不会对公司损益产生负面影响,但本次判决为一审判决,尚在上诉期。公司将密切关注案件后续情况并及时履行信息披露义务。
2024-01-23 20:17
【益方生物:2023年预亏2.89亿元 同比减亏】益方生物(688382)1月23日晚间公告,公司预计2023年度净利润亏损2.89亿元,与上年同期相比,亏损额减少了1.94亿元。报告期内,公司的主要产品仍处于研发阶段,尚未进行商业化生产和销售,因此没有实现产品销售收入。然而,公司的技术许可和合作收入相比上年同期有所增加,这将减少亏损幅度。
2024-01-02 22:06
【益方生物:格舒瑞昔片新药上市申请获受理】益方生物1月2日晚间公告,公司近日收到国家药监局核准签发的《受理通知书》,公司产品格舒瑞昔片用于既往经一线系统治疗后疾病进展或不可耐受的、并且经检测确认存在KRASG12C突变的局部晚期或转移性非小细胞肺癌的治疗的新药上市申请获得受理。
2024-01-02 16:20
益方生物:格舒瑞昔片新药上市申请获得受理
2023-11-02 17:21
【益方生物:收到美国新泽西地区法院书面文件】《科创板日报》2日讯,益方生物公告,近日,公司收到美国新泽西地区法院书面文件,Beta Pharma,Inc.(简称“美国倍而达”)在美国新泽西地区法院对公司、Yueheng Jiang(江岳恒)、Wansheng Jerry Liu和Fox Rothschild,LLP提起了民事诉讼。美国倍而达提出,公司的申请号为CN201910491253.6的专利申请存在联邦《保护商业秘密法》和《新泽西州商业秘密法》项下的商业秘密盗窃,以及与美国倍而达声称的保密和专有的涉诉化合物相关的商业秘密盗用、对于违反受托义务的协助和教唆、不当得利、不正当竞争、民事共谋等情况。美国倍而达据此请求法院,要求赔偿其损失,并要求公司将包括涉案专利申请在内的相关专利及专利申请的权利人变更登记为原告。
2023-09-17 16:47
【益方生物:正开展联用辉瑞CDK4/6抑制剂哌柏西利的临床试验,目前处于临床Ib期】益方生物近期接受投资者调研时称,公司在国内目前正在开展的是与氟维司群(Fulvestrant)头对头的二线注册临床三期试验。同时,公司还在开展联用辉瑞CDK4/6抑制剂哌柏西利的临床试验,目前处于临床Ib期。D-0502已在去年四季度开始入组患者,今年主要任务是将全力入组主要患者,并于明年完成患者入组。
2023-08-03 16:33
益方生物:与正大天晴签署许可与合作协议,公司授予正大天晴在协议期限内对益方生物D-1553产品在中国大陆地区开发、注册、生产和商业化的独家许可权。正大天晴将向公司支付最高不超过人民币5.5亿元的首付款及里程碑款;并按年净销售额向公司分层支付特许权使用费。
2023-07-24 19:00
【益方生物:D-0502将于明年完成患者入组】益方生物披露调研纪要显示,公司在国内目前正在开展的是与氟维司群(Fulvestrant)头对头的二线注册临床三期试验。同时,公司还在开展联用辉瑞CDK4/6抑制剂哌柏西利的临床试验,目前处于临床Ib期。D-0502已在去年四季度开始入组患者,今年主要任务是将全力入组主要患者,并于明年完成患者入组。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 掌握四大技巧,精准判断股市上涨空间
- 股市智慧:掌握十不下单原则,稳健投资之道
- 掌握强势股加仓六大黄金信号,精准捕捉股市机遇
- 股市智慧:顶尖操盘手的心得与策略解析
- 股市短线秘籍:15分钟K线超短线作战法深度剖析
- 股票投资的智慧:精准逢高卖出的策略与实践
- 主力高位出货策略的深度剖析与防范
- 操盘手的智慧:掌握六大铁律,解锁股市解套秘籍
- 揭秘职业操盘手的资金运作之道
- 补仓的艺术:从失败到成功的实战策略分析
- 散户炒股的智慧:挖掘并发挥散户优势
- 四步策略,打造短线炒股高手之路
- 识破股市迷雾:全面解析空头陷阱识别策略
- 换手率:股市选股的重要指标
- ST股票运行规律与投资机遇探秘
- 揭秘成交量选股法:洞悉市场动向,把握投资先机
- 成都股民老曾的股市传奇:八年资产暴增58倍的智慧与坚持
- 揭秘股市亏损的典型原因
- 成交量决定股价:深度解析九句口诀的股市智慧
- 左肩与右肩:抄底逃顶的智慧对决
当前版本:V3.0

 VIP复盘网
VIP复盘网
