
扫码关注公众号
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
浙江医药
600216 |
-1.67%
|
最新:13.51
开盘:13.72 昨收:13.74 |
开盘%:-0.15%
振幅%:1.6% 换手%:1.45% |
最高:13.72
最低:13.5 量比:1.01 |
总市值:130 亿
流通值:130 亿 成交额:10 亿 |
- 基本信息
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- Deepseek分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
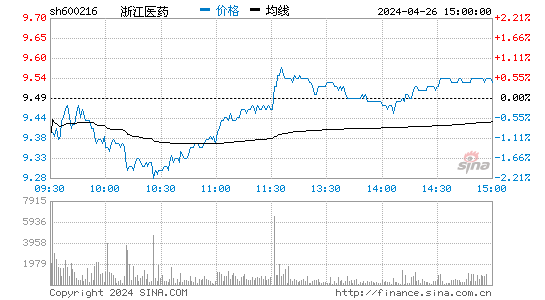
- 分时图
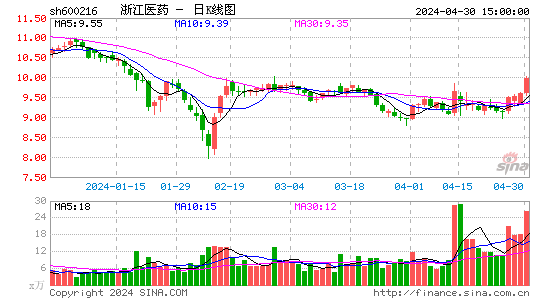
- 日K图
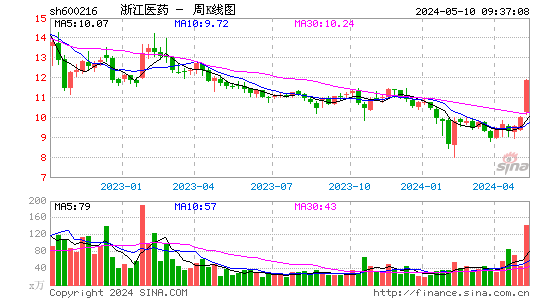
- 周K图
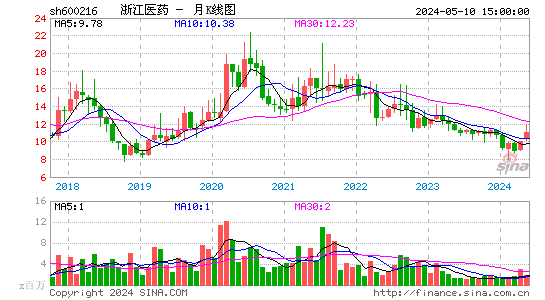
- 月K图
浙江医药股票概况
全面了解浙江医药及其股票投资价值
公司概况
浙江医药股份有限公司是一家总部位于中国的综合性医药企业,致力于药品研发、生产和销售。公司自成立以来,凭借强大的研发实力和丰富的产品线,在国内外医药市场上占据了一席之地。
业务领域
药品研发:浙江医药在抗肿瘤、抗感染、心血管等多个治疗领域拥有自主研发的核心产品。公司不断加大研发投入,推动新药研发进程,以满足市场需求。
药品生产:公司拥有现代化的生产基地和严格的质量控制体系,确保药品的安全性和有效性。
药品销售:浙江医药的销售网络遍布国内外,与多家医疗机构和药店建立了长期合作关系。
财务分析
从近年来的财务数据来看,浙江医药的经营业绩保持稳定增长。公司的营业收入和净利润均呈现出上升趋势,显示出良好的盈利能力。
市场前景
随着国内医药市场的不断扩大和人口老龄化趋势的加剧,浙江医药的市场前景广阔。公司将继续加大研发投入,拓展产品线,提升市场竞争力。
总结
浙江医药作为一家综合性医药企业,在药品研发、生产和销售等方面均表现出色。其股票在市场上具有较高的投资价值,值得投资者关注。
以上内容仅供参考,不构成投资建议。投资者应结合自身风险承受能力和投资目标,谨慎决策。
2025-03-20 20:24
浙江医药:国投高科拟拟减持不超过1%
2025-02-27 16:00
浙江医药:复方醋酸钠林格注射液获得药品注册证书
2025-02-26 15:32
【浙江医药:子公司创新生物通过美国FDA现场检查】2月26日电,浙江医药公告称,公司控股子公司浙江创新生物有限公司于2024年10月30日至11月8日接受了美国FDA的CGMP现场检查,检查范围为注射用盐酸万古霉素。近日,创新生物收到FDA签发的现场检查报告及信函,确认创新生物的生产质量管理体系符合美国FDA的CGMP要求,顺利通过本次日常监督检查。此次通过FDA检查,提升了浙江医药制剂产品的国际竞争力,为其他产品推向国际市场奠定了基础。
2024-12-12 16:35
【最卷品类西格列汀口服常释剂型33进9 惠升生物第一顺位拟中标】12月12日电,记者在第十批国采开标现场获悉,本次集采中有33家企业竞标西格列汀口服常释剂型,结果显示共有9家企业拟中标,按顺位分别是惠升生物、江苏万邦生化、宁波美舒医药科技、重庆圣华曦、浙江医药、江西施美、江苏德源、常州制药厂以及浙江诺得。小财注:据药智数据显示,2023年西格列汀口服常释剂型在国内公立医院的销售额为26.56亿元,默沙东占据了99.65%的市场份额。(记者卢阿峰 何凡)
2024-11-11 20:35
【浙江医药:国投高科拟减持不超过1%公司股份】11月11日电,浙江医药公告,公司股东国投高科拟通过集中竞价交易方式合计减持数量不超过961.64万股,即不超过公司总股本的1%。
2024-10-24 15:39
【浙江医药:第三季度净利润同比增长1737.57%】浙江医药公告,2024年第三季度,公司实现营业收入27.07亿元,同比增长39.66%。归属于上市公司股东的净利润为5.34亿元,同比增长1737.57%。年初至报告期末,公司实现营业收入71.13亿元,同比增长21.04%;净利润为8.5亿元,同比增长181.96%。本报告期营业收入、净利润上涨主要系公司主导产品维生素 E、维生素 A 销量和价格上涨所致。
2024-08-22 15:36
浙江医药半年报:上半年实现营业收入44.05亿元,同比增长11.87%,实现归属于母公司股东净利润3.15亿元,同比增长15.82%。
2024-08-14 16:25
【浙江医药:注射用达托霉素获得药品注册证书】8月14日电,浙江医药公告,公司近日收到国家药品监督管理局核准签发的注射用达托霉素(0.5g)的《药品注册证书》。控股子公司昌海制药收到国家药品监督管理局核准签发的替考拉宁《化学原料药上市申请批准通知书》。
2024-05-27 16:54
浙江医药:获得注射用LYSC98药物临床试验批准通知书。
2024-04-29 15:44
浙江医药:子公司收到恩格列净化学原料药上市申请批准通知书
2023-11-27 16:23
浙江医药:SH-337片获得药物临床试验批准通知书
2023-11-27 16:20
【浙江医药:SH-337片获得药物临床试验批准通知书】浙江医药公告,收到国家药品监督管理局核准签发关于SH-337片的《药物临床试验批准通知书》,经审查,SH-337片临床试验申请符合药品注册的有关要求,同意本品开展临床试验。
2023-10-20 15:56
浙江医药:子公司收到达托霉素化学原料药上市申请批准通知书
2023-09-18 15:49
【浙江医药:获得注射用NCB003药物临床试验批准通知书】9月18日电,浙江医药公告,下属子公司浙江新码生物医药有限公司收到国家药品监督管理局下发的关于公司在研药物注射用NCB003的《药物临床试验批准通知书》,同意本品单药在晚期实体瘤开展临床试验。
2023-08-30 16:21
浙江医药:子公司收到盐酸米诺环素化学原料药上市申请批准通知书
2023-08-18 15:19
【浙江医药:近期信托产品爆雷事件对公司并无重大影响】浙江医药在互动平台表示,近期信托产品爆雷事件对公司并无重大影响。
2023-06-30 20:09
【浙江医药:子公司昌海制药通过美国FDA现场检查】浙江医药(600216)6月30日晚间公告,6月29日,昌海制药收到FDA的通知函和针对本次检查签发的现场检查报告,FDA确认本次检查已结束。该通知说明昌海制药的质量管理体系符合美国FDA的标准,顺利通过了本次美国FDA现场检查。检查内容为盐酸米诺环素原料药的批准前检查和达托霉素原料药的日常监督检查。
2023-04-24 15:34
浙江医药:拟将下属分公司维生素厂坐落于绍兴袍江斗门街道丁港、东堰地段的房屋、土地以及上述不动产范围内的附属设施、设备等资产转让给绍兴袍江创业建设发展有限公司,转让价格按照政府征收补偿标准执行,合计金额为4亿元
2023-03-30 15:56
浙江医药:苹果酸奈诺沙星胶囊获得药物临床试验批准通知书
2023-02-21 15:43
浙江医药:公司药品黄体酮软胶囊通过仿制药一致性评价
2023-01-18 17:02
浙江医药:预计2022年净利润为4.73亿元-5.78亿元,同比减少44.67%-54.72%。公司主导产品维生素E、维生素A销量下滑,其中维生素A价格下降幅度较大;主导产品左氧氟沙星氯化钠注射液进入全国集采后销售价格和毛利大幅下降
2023-01-16 21:07
【浙江医药:苹果酸奈诺沙星制剂进入医保后销量增长较快】浙江医药(600216)1月16日在互动平台表示,公司苹果酸奈诺沙星制剂进入医保后销售量和销售额增长较快。
2022-10-31 16:51
【浙江医药:获得药物临床试验批准通知书】10月31日电,浙江医药公告,近日,公司下属子公司浙江新码生物医药有限公司收到国家药品监督管理局核准签发的注射用重组人源化抗HER2单抗-AS269偶联物(ARX788)《药物临床试验批准通知书》,同意开展用于评价ARX788在HER2阳性胆道癌患者中有效性及安全性的II期临床研究。
2022-10-31 16:49
浙江医药:收到国家药品监督管理局核准签发的注射用重组人源化抗HER2单抗-AS269偶联物(ARX788)《药物临床试验批准通知书》。
2022-10-20 13:49
【浙江医药:钠离子电解液生产线正在研究规划之中】浙江医药在互动平台表示,ARX788治疗乳腺癌三期临床于2022年5月份完成病例入组,原计划在苏州举行的创新大会上发布部分中期数据,因该会议推迟至2022年11月上旬召开,故发布时间推迟。公司钠离子电解液生产线正在研究规划之中。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 识破股市迷雾:精准捕捉空头陷阱的策略
- 短线交易的盈利迷思与资金管理策略探索
- 炒股攻略:尾盘选牛股战法与趋势解读,把握市场盈利金钥匙
- 知足者常乐:期货交易中的智慧与贪婪博弈
- 交易的十个深刻真相:解锁盈利之门
- 高手选股秘籍:六大法则深度剖析
- 股票交易中的智慧:论等待的重要性与投资策略
- 洞悉市场脉搏:深入解析DDX指标与大单动向
- 股市迷雾中的明灯:用市场估值智慧精准捕捉“顶”与“底”
- 股民炒股的五个成长阶段:从懵懂到成精的蜕变
- 揭秘股市神秘法则:黄金分割线与涨停策略
- 把握多头市场节奏:各阶段的投资策略解析
- 揭秘龙头股的崛起之路:深度剖析十一大核心特征
- 深度解析优先股:权利、特征与投资策略
- 捕捉股市低吸黄金点,五种经典形态深度剖析
- 股市买卖九大法则深入解析
- 高手策略:暴跌行情中的智慧应对与机遇把握
- 巴菲特投资智慧:守护本金,稳健前行
- 散户股市迷思:揭秘“一买就跌,一卖就涨”的背后真相
- 尾盘选股的艺术:精准捕捉强势股秘籍
当前版本:V3.0

 VIP复盘网
VIP复盘网
