
扫码关注公众号
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
复星医药
600196 |
-1.2%
|
最新:25.44
开盘:25.78 昨收:25.75 |
开盘%:0.12%
振幅%:1.51% 换手%:0.68% |
最高:25.79
最低:25.4 量比:0.75 |
总市值:680 亿
流通值:539 亿 成交额:21 亿 |
- 基本信息
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- Deepseek分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
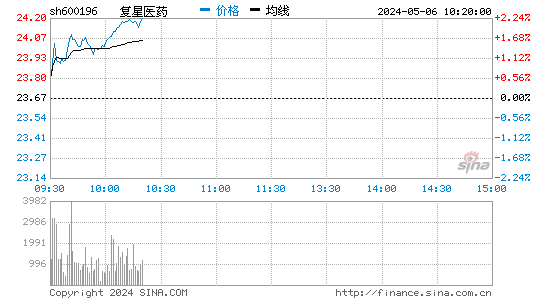
- 分时图
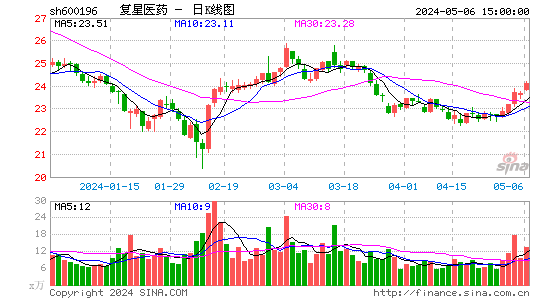
- 日K图
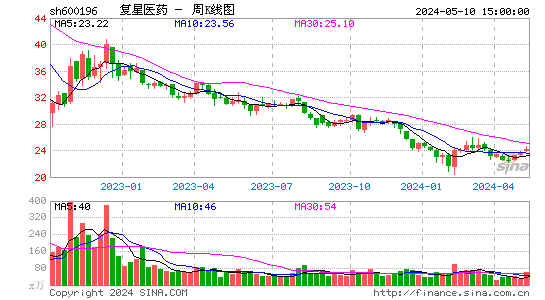
- 周K图
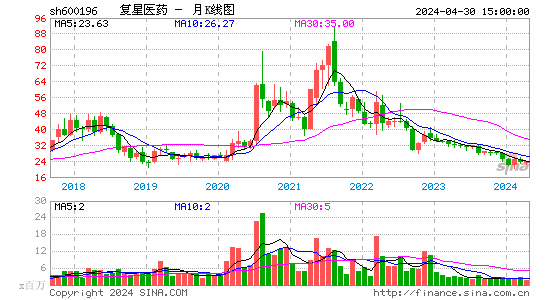
- 月K图
复星医药股票概况
了解全球化医药健康产业集团的股市表现
一、公司概况
复星医药(600196.SH,02196.HK)成立于1994年,是一家植根中国、创新驱动的全球化医药健康产业集团。其业务范围涵盖制药、医疗器械与医学诊断、医疗健康服务等领域,并通过参股国药控股扩展到医药商业领域。
二、股市表现
截至2025年2月10日,复星医药A股收盘价为25.43元,港股收盘价为14.840港元。股价呈现波动性,但整体呈现上升趋势,显示出市场对复星医药的信心。
三、主营业务
制药业务:作为公司的核心业务,包括创新药、成熟产品及制造业务、疫苗业务。其中,创新药业务聚焦肿瘤、免疫等核心治疗领域。
医疗器械与医学诊断:构建以医疗美容、呼吸健康等为核心的三大业务分支。
医疗健康服务:形成线上线下一体化的医疗服务平台。
四、财务状况
复星医药的资产负债率维持在48.64%左右,财务状况稳定。营业收入和归母净利润持续增长,显示出良好的盈利能力和销售毛利率。
五、创新与发展
复星医药在创新药方面增长动能强劲,业务结构持续优化。公司积极推动优质产品出海,不断提升国际声誉和市场份额。
总结
复星医药作为全球化医药健康产业集团的佼佼者,以其稳健的股市表现、多元化的业务布局、良好的财务状况以及持续的创新与发展,赢得了市场和投资者的广泛认可。未来,随着全球医疗健康市场的不断发展,复星医药有望继续保持强劲的增长势头。
2025-03-31 19:01
复星医药:公司、国际金融公司(IFC)、亚洲开发银行(ADB)拟各自出资人民币2.7亿元(或等值美元)分别认购联合健康险105,468,750股新增发行股份(对应新增注册资本人民币105,468,750元)。本次增资完成后,本公司持有联合健康险的股权比例将由14.00%增至20.05%。
2025-03-25 21:28
【复星医药:2024年净利润同比增长16.08%,拟10派3.2元】复星医药公告,2024年实现营业收入410.67亿元,同比下降0.80%;归母净利润27.7亿元,同比增长16.08%。公司拟每10股派发现金红利3.2元(含税)。报告期内,公司进一步聚焦创新药和高值器械,推进产品结构和策略转型。创新产品收入稳步增长,核心品种创新型抗PD-1单抗斯鲁利单抗注射液(中国境内商品名:汉斯状)、CAR-T细胞治疗产品奕凯达(阿基仑赛注射液)、止吐药物奥康泽(奈妥匹坦帕洛诺司琼胶囊)以及长效重组人粒细胞集落刺激因子产品珮金(拓培非格司亭注射液)、心衰和高血压治疗药物一心坦(沙库巴曲缬沙坦钠片)均实现较快增长。
2025-03-25 21:13
【复星医药:控股子公司获药品临床试验批准】3月25日电,复星医药(600196.SH)公告称,公司控股子公司上海复宏汉霖生物技术股份有限公司及其控股子公司收到国家药监局关于同意HLX79注射液联合利妥昔单抗注射液用于治疗活动期肾小球肾炎开展临床试验的批准。复宏汉霖拟于条件具备后于中国境内开展该药品的II期临床试验。截至2025年2月,本集团现阶段针对该治疗方案的累计研发投入约为人民币14万元。
2025-03-19 17:06
复星医药:控股子公司药品HLX22(重组人源化抗HER2单克隆抗体注射液)获美国FDA孤儿药资格认定
2025-03-14 08:42
【复星医药与赛陆医疗达成战略合作】3月13日,复星医药与赛陆医疗达成战略合作,双方将在产品研发、平台搭建、应用推广等方面开展全方位、深层次的合作,共同推动医疗行业的创新与发展。(证券时报)
2025-03-13 17:42
复星医药:控股子公司复星实业拟以现金12,408万美元的对价向Calcite Gem转让其所持有的标的公司(其主要资产系其通过其控股子公司NFH持有及运营的“和睦家”医院和诊所)940万股普通股;本次交易完成后,本集团将不再持有标的公司的股权
2025-03-06 17:56
【复星医药:药品丁二酸复瑞替尼胶囊注册申请获受理】3月6日电,复星医药(600196.SH)公告称,控股子公司复星万邦就丁二酸复瑞替尼胶囊(SAF-189)的药品注册申请获国家药品监督管理局受理。该新药为创新型小分子化学药物,拟用于治疗非小细胞肺癌(ALK+)、非小细胞肺癌(ROS1+)等。截至2025年1月,累计研发投入约为4.39亿元。该新药在ALK阳性的非小细胞肺癌晚期患者中展现出良好的临床疗效,对中枢神经系统转移灶疗效显著,且安全性良好。
2025-03-04 16:58
复星医药:控股子公司获24价肺炎球菌多糖结合疫苗临床试验批准。
2025-03-04 16:58
【复星医药:控股子公司获24价肺炎球菌多糖结合疫苗临床试验批准】3月4日电,复星医药(600196.SH)公告称,公司控股子公司复星安特金收到国家药监局关于24价肺炎球菌多糖结合疫苗的临床试验批准。该疫苗为本集团自主研发的预防用生物制品,拟用于预防由肺炎球菌血清型引起的感染性疾病。复星安特金拟于条件具备后在中国境内开展该疫苗的I期临床试验。截至2025年1月,本集团针对该疫苗的累计研发投入约为人民币0.44亿元。根据目前中国境内关于疫苗产品的审批要求,该疫苗尚需完成相关临床试验、生产设施通过GMP符合性检查和注册现场核查等注册申报环节,并获得上市注册批准后,方可上市。
2025-02-27 16:54
【复星医药:控股子公司获药品临床试验批准】2月27日电,复星医药公告称,控股子公司江苏星盛新辉医药有限公司收到国家药品监督管理局关于同意XS-03片与FOLFOX或FOLFIRI和贝伐珠单抗联合用于治疗RAS突变转移性结直肠癌临床试验的批准。星盛新辉拟于条件具备后于中国境内开展该治疗方案的Ib/II期临床试验。XS-03为复星医药自主研发的小分子口服PLK1抑制剂,主要通过抑制细胞周期调节因子,诱导有丝分裂阻滞,达到抑制肿瘤细胞增殖、促进肿瘤细胞凋亡的抗肿瘤作用。截至本公告日期,XS-03单药用于治疗RAS突变晚期实体瘤于中国境内处于I期临床试验阶段。
2025-02-26 17:25
【复星医药:盐酸替那帕诺片上市许可申请获批】复星医药公告,公司控股子公司上海复星医药产业发展有限公司获许可产品盐酸替那帕诺片(中国境内商品名:万缇乐®)的上市许可申请近日获国家药监局批准,此次获批适应症为用于控制对磷结合剂疗效不充分或不耐受的慢性肾脏病(CKD)成人透析患者的血清磷水平。另外,公司控股子公司苏州二叶制药有限公司就复方匹可硫酸钠颗粒的上市注册申请近日获国家药监局批准。该药品主要用于结肠镜检查、X射线检查前的肠道清洁准备,用于必要时在外科手术前清洁肠道。
2025-02-14 23:11
【复星医药:深度拥抱AI,自研PharmAID决策智能体平台助力高效创新】2月14日,复星医药在投资者互动平台上表示,公司高度重视且密切关注人工智能(AI)技术在医药医疗领域的变革潜力,目前已开展多项应用和尝试。公司近期在内部发布了自主研发的PharmAID决策智能体平台,构建起覆盖创新研发场景的全生命周期智能决策网络。该平台深度融合全球领先的大模型技术,并已率先接入Deepseek-R1,基于PharmAID决策智能体平台,复星医药正加速推进“药物商业价值辅助决策”的能力建设,提升决策视野,提高决策准确性。
2025-02-10 16:58
复星医药:控股子公司桂林南药股份有限公司就注射用硫酸多黏菌素B、上海朝晖药业有限公司就盐酸拉贝洛尔注射液的药品注册上市申请已分别获国家药品监督管理局受理
2025-02-10 16:58
复星医药:复宏汉霖于近日收到美国FDA关于同意HLX99开展临床试验的批准
2025-02-06 18:55
复星医药:复宏汉霖与Dr.Reddy’s签订《许可协议》,由复宏汉霖就在研产品HLX15(即重组抗CD38全人单克隆抗体注射液)的静脉注射制剂(IV)与皮下注射制剂(SC)剂型授予Dr.Reddy’s于许可区域(即美国及约定的欧洲地区<包括英国、瑞士等42个欧洲国家>)及许可领域(即各约定参比制剂于许可区域内各国家获批上市之适应症)内的开发、生产及商业化权利的许可
2025-02-06 18:54
复星医药:控股子公司星浩澎博于近日收到国家药品监督管理局关于同意XH-S004片用于治疗慢性阻塞性肺疾病的临床试验批准
2025-02-05 18:58
【复星医药:控股子公司药品斯鲁利单抗注射液成为首个欧盟批准用于广泛期小细胞肺癌治疗的抗PD-1单抗】复星医药公告,本公司控股子公司上海复宏汉霖生物技术股份有限公司及其控股子公司自主研发的斯鲁利单抗注射液(即抗 PD-1 单抗,欧盟商品名:Hetronifly®)联合卡铂和依托泊苷适用于广泛期小细胞肺癌(ES-SCLC)成人患者的一线治疗的上市许可申请(MAA)于近日获欧盟委员会(即 European Commission)批准。据此,该药品获得所有欧盟成员国及冰岛、列支敦士登和挪威(分别为欧洲经济区
2025-01-22 19:06
【复星医药:吸收合并控股子公司复宏汉霖将不予实施】1月22日,吸收合并作为特别决议案于复宏汉霖临时股东大会上获出席会议的三分之二以上(含本数)有表决权股东的批准,但于仅由独立H股股东享有表决权的复宏汉霖H股类别股东大会上未获通过,因此,本次交易协议的生效条件未获达成,吸收合并将不予实施,复宏汉霖将保留H股上市地位。
2025-01-22 18:59
复星医药:拟以3亿元-6亿元回购股份A股股份,A股回购价格上限为人民币30元/股;拟以自有资金及/或自筹资金回购H股,回购H股股数不超过2023年度股东大会决议日(即2024年6月26日)本公司H股总数的5%
2025-01-20 16:24
复星医药:控股子公司获重酒石酸间羟胺注射液药品注册批准。
2025-01-14 17:58
【复星医药:控股子公司药品XH-S003胶囊启动II期临床试验】1月14日电,复星医药公告,控股子公司浙江星浩澎博医药有限公司就XH-S003胶囊启动II期临床试验,该药品用于治疗IgA肾病等补体异常激活相关的肾小球疾病。XH-S003是集团自主研发的小分子抑制剂,拟用于治疗补体异常激活相关的疾病。临床前研究显示,XH-S003在相关肾小球肾病动物模型中可以显著降低因补体激活导致的炎性损伤、改善肾功能,且表现出良好的安全性。截至2024年11月,集团针对XH-S003累计研发投入约为人民币0.98亿元。XH-S003尚需在中国境内开展一系列临床研究并经国家药品审评部门审批通过后,方可上市。新药研发及至上市存在诸多不确定因素,投资者注意投资风险。
2025-01-09 17:28
复星医药:控股子公司获枸橼酸伏维西利胶囊药品注册申请受理
2025-01-02 16:19
复星医药:控股子公司获注射用雷替曲塞药品注册申请受理
2024-12-06 15:42
【复星医药投资成立新公司 含企业管理业务】企查查APP显示,近日,上海星韬生物医药有限责任公司成立,法定代表人为李川,注册资本为1万元,经营范围包含:医学研究和试验发展;企业管理;企业管理咨询。企查查股权穿透显示,该公司由复星医药间接全资持股。
2024-12-04 17:05
复星医药:控股子公司复宏汉霖获帕妥珠单抗生物类似药HLX11(重组抗HER2结构域II人源化单克隆抗体注射液)药品注册申请受理
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 识破股市迷雾:精准捕捉空头陷阱的策略
- 短线交易的盈利迷思与资金管理策略探索
- 炒股攻略:尾盘选牛股战法与趋势解读,把握市场盈利金钥匙
- 知足者常乐:期货交易中的智慧与贪婪博弈
- 交易的十个深刻真相:解锁盈利之门
- 高手选股秘籍:六大法则深度剖析
- 股票交易中的智慧:论等待的重要性与投资策略
- 洞悉市场脉搏:深入解析DDX指标与大单动向
- 股市迷雾中的明灯:用市场估值智慧精准捕捉“顶”与“底”
- 股民炒股的五个成长阶段:从懵懂到成精的蜕变
- 揭秘股市神秘法则:黄金分割线与涨停策略
- 把握多头市场节奏:各阶段的投资策略解析
- 揭秘龙头股的崛起之路:深度剖析十一大核心特征
- 深度解析优先股:权利、特征与投资策略
- 捕捉股市低吸黄金点,五种经典形态深度剖析
- 股市买卖九大法则深入解析
- 高手策略:暴跌行情中的智慧应对与机遇把握
- 巴菲特投资智慧:守护本金,稳健前行
- 散户股市迷思:揭秘“一买就跌,一卖就涨”的背后真相
- 尾盘选股的艺术:精准捕捉强势股秘籍
当前版本:V3.0

 VIP复盘网
VIP复盘网
