
扫码体验VIP

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
华东医药
000963 |
2.31%
|
最新:43.38
开盘:42.4 昨收:42.4 |
开盘%:0%
振幅%:3.84% 换手%:0.99% |
最高:43.88
最低:42.25 量比:1.63 |
总市值:761 亿
流通值:760 亿 成交额:18 亿 |
- 基本信息
- 主力分时图 New
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
- 分时图
- 日K图
- 周K图
- 月K图
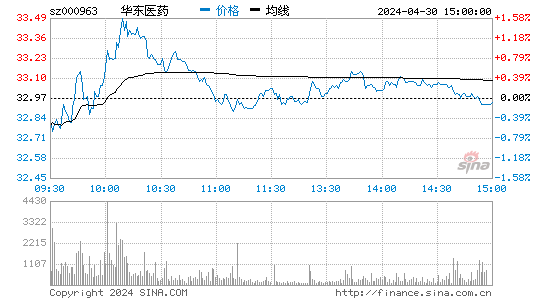
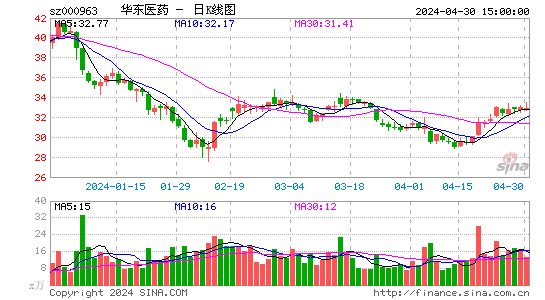
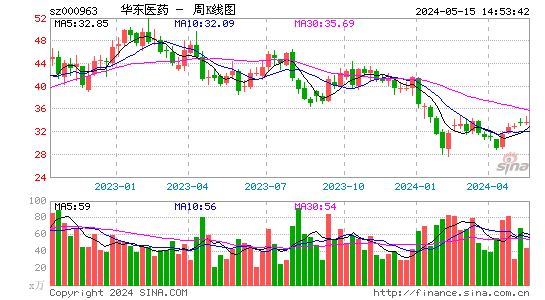
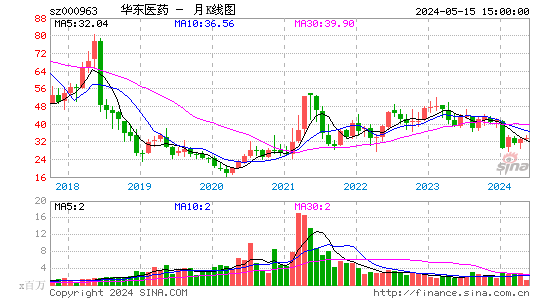
华东医药股票概况
全面了解华东医药及其股市表现
公司概况
华东医药是一家集医药研发、生产、销售于一体的大型综合性制药企业。公司主要产品涵盖化学原料药、化学制剂药、中成药、生物药品等多个领域,并在国内外市场上占据重要地位。
股票表现
华东医药的股票在深交所上市,股票代码为000963。近年来,公司股价呈现波动上涨的趋势。截至最新数据,华东医药的股权质押总比例为8.38%,质押总股数为1.47亿股。
业务领域
化学制药:华东医药在化学制药领域拥有强大的研发和生产能力,产品涵盖了抗生素、心血管药物等多个治疗领域。
医疗器械:公司在医疗器械领域也有涉足,全资子公司曾收到医疗器械注册申请受理通知书,展现了其在该领域的布局。
市场表现与业绩
华东医药的业绩表现稳定,净利润持续增长。公司的总市值也呈现出稳步增长的趋势。
总结
华东医药作为化学制药行业的佼佼者,在多个领域都有卓越表现。其股票在股市中也备受投资者关注。未来,华东医药有望继续保持稳定增长,为投资者带来丰厚回报。
总结:华东医药在化学制药和医疗器械领域拥有强大的研发和生产能力,业绩表现稳定,股价波动上涨。投资者可关注其股市表现,把握投资机会。
2025-07-28 17:19
【华东医药:全资子公司获得MC2-01乳膏药物临床试验批准通知书】7月28日电,华东医药(000963.SZ)公告称,全资子公司杭州中美华东制药有限公司收到国家药品监督管理局核准签发的MC2-01乳膏治疗中国斑块状银屑病的Ⅲ期临床试验批准通知书。MC2-1乳膏是卡泊三醇和倍他米松的固定剂量复方制剂,用于局部治疗成人斑块状银屑病,包括头皮银屑病。本品利用MC2独有的药物递送系统PAD™技术,使其成为一种方便使用的水性乳膏。本品于2020年在美国获得FDA批准,2021年在欧洲获批,并于2024年11月在澳大利亚获批上市。此次批准是该产品研发进程中的重要里程碑,将进一步提升公司在自身免疫领域和皮肤外用制剂领域的核心竞争力。
2025-07-23 15:48
【华东医药:全资子公司HDM1002片获得美国FDA临床试验批准通知】7月23日电,华东医药(000963.SZ)公告称,公司全资子公司中美华东收到美国FDA通知,由中美华东申报的HDM1002片药品临床试验申请已获得FDA批准。HDM1002片为中美华东自主研发并拥有全球知识产权的创新型小分子药物,具有口服活性、强效、高选择性的GLP-1受体小分子完全激动剂,可强效激活GLP-1受体,诱导环磷酸腺苷(cAMP)产生,具有强效的改善糖耐受、降糖和减重作用。该产品中国I期及II期临床试验累计入组超过800例受试者,已有数据显示其在体重减轻和血糖控制方面有显著疗效。此次获得临床试验批准对公司近期业绩不会产生重大影响,药品研发存在投入大、周期长、风险高等特点,未来产品市场竞争形势存在不确定性。
2025-07-22 10:03
【世界卫生组织:基于GLP-1疗法治疗成人肥胖症的新指南计划9月份正式发布】7月22日电,记者获悉,世界卫生组织(WHO)正在制定的基于GLP-1的疗法治疗成人肥胖症的新指南,计划于2025年9月正式发布。该指南由独立的指南开发小组(GDG)负责制定,小组成员包括肥胖领域的专家、流行病学专家、临床管理专家、药理学家、卫生经济学家、公共卫生项目专家以及政策制定者,以确保指南符合世界卫生组织的严格标准。据悉,该指南的目的在于明确GLP 1 RAs的临床适应症、应用以及规划方面的考量。该指南有望成为世界卫生组织首次正式推荐使用减肥药物治疗成人肥胖症。此举标志着该全球卫生机构在应对日益严重的肥胖危机方面政策的重大转变。 (证券时报)
2025-07-18 15:51
【华东医药:全资子公司全球首创的1类生物制品注射用HDM2012临床试验获批】7月18日电,华东医药(000963.SZ)公告称,公司全资子公司中美华东收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,注射用HDM2012临床试验申请获得批准。该药物是由中美华东自主研发的靶向人粘蛋白-17的新型抗体药物偶联物,属于全球首创的1类生物制品。临床前研究结果显示,HDM2012具有良好的成药性、安全性和有效性。本次临床试验获批是该产品研发进程中的重要进展,将进一步提升公司在肿瘤治疗领域的核心竞争力。但需注意,药物在获得临床试验批准通知书后,尚需完成后续临床试验并经国家药品监督管理局审评、审批通过后方可上市。
2025-07-14 17:43
华东医药:全资子公司注射用HDM2020获得美国FDA新药临床试验批准通知。
2025-07-14 09:43
【国产减重新药在深圳开出首张处方】7月14日电,近日,深圳前海泰康医院减重中心连续为两位肥胖合并代谢性疾病患者开具国产减重新药玛仕度肽和替尔泊肽处方,成为深圳市首家应用这两款创新药物的医疗机构。玛仕度肽是全球首个GLP-1(胰高血糖素样肽-1)/GCG(胰高血糖素)双受体激动剂减重药物,通过双重调节机制增强能量消耗与食欲控制。替尔泊肽则是国内首个GLP-1/GIP(葡萄糖依赖性促胰岛素多肽)双靶点药物,兼具降糖与减重功效。两款药物通过多通路协同作用,显著提升减重效果,尤其适合传统方法无效的顽固性肥胖患者。(深圳晚报)
2025-06-30 20:55
【华东医药:全资子公司获得美国FDA新药临床试验批准通知】华东医药6月30日公告,全资子公司杭州中美华东制药有限公司收到美国食品药品监督管理局(FDA)通知,由中美华东申报的注射用HDM2012药品临床试验申请已获得美国FDA批准,可在美国开展I期临床试验,适应症为晚期实体瘤。
2025-06-30 20:51
华东医药:由中美华东申报的注射用HDM2012药品临床试验申请已获得美国FDA批准,可在美国开展I期临床试验,适应症为晚期实体瘤。
2025-06-26 18:34
【华东医药:子公司注射用HDM2020临床试验获批】6月26日电,华东医药(000963)6月26日晚间公告,6月25日,公司全资子公司中美华东收到国家药监局核准签发的《药物临床试验批准通知书》,由中美华东申报的注射用HDM2020临床试验申请获得批准。临床前研究已证明HDM2020在靶点阳性的胃癌、鳞状非小细胞肺癌等药效模型中显示出强大的抗肿瘤活性,具有良好的成药性和安全性。
2025-06-20 17:01
【华东医药:爱拉赫®和炎朵®预计今年下半年起陆续在国内正式商业化销售】6月20日电,有投资者问,公司去年获批的创新药爱拉赫以及炎朵预计国内什么时候正式上市销售?华东医药在互动平台表示,爱拉赫®和炎朵®预计于今年下半年起陆续开始在国内正式商业化销售。
2025-06-09 16:55
【华东医药:全资子公司收到美国FDA新药临床试验批准通知】6月9日电,华东医药(000963.SZ)公告称,公司全资子公司中美华东收到美国FDA通知,由中美华东申报的HDM1010片药品临床试验申请已获得美国FDA批准,可在美开展I期临床试验,适应症为2型糖尿病。
2025-06-02 17:30
【华东医药:雷珠单抗注射液上市许可申请获受理】6月2日电,华东医药(000963)6月2日晚间公告,公司全资子公司中美华东收到国家药监局签发的受理通知书,由中美华东申报的雷珠单抗注射液上市许可申请获得受理。雷珠单抗注射液用于治疗湿性(新生血管性)年龄相关性黄斑变性(AMD)等。
2025-05-12 18:05
华东医药:控股子公司DR10624的临床研究结果在2025年欧洲肝病研究学会(EASL)年会发布
2025-04-30 13:12
创新药概念持续活跃,百济神州、诺诚健华、锦波生物均创出历史新高,科伦药业、益方生物、泽璟制药、华东医药、恒瑞医药等涨幅靠前
2025-04-18 09:28
A股减肥药概念盘初活跃,金凯生科涨超10%,昊帆生物、华东医药、翰宇药业、百花医药、一品红、常山药业等集体高开。
2025-04-07 17:35
华东医药:控股子公司获得注射用DR30206药物临床试验批准通知书
2025-04-01 16:54
华东医药:全资子公司收到司美格鲁肽注射液药品注册受理通知书
2025-03-31 19:38
【荃信生物:预计2025年赛乐信销售额将达3亿元】3月31日电,荃信生物在今日举行的2024年度业绩会中表示,赛乐信®作为生物类似药已自动进入医保目录,同时叠加华东医药较强的销售能力,预计2025年该产品销售额将达3亿元,峰值为15亿元-20亿元,该产品产生销售利润后,荃信生物取得的分成将计入公司收入。公司副总经理林伟栋表示,目前公司在朝着2025年整体收入2亿元的目标推进,“一块是我们最大的BD收入,一块是赛孚士CDMO的收入,第三块是我们乌司奴单抗生物类似药的供货收入。”小财注: 赛乐信®作为荃信生物产品管线中首个商业化产品,于2024年10月获批上市,是国内首个获批的乌司奴单抗注射液生物类似药。2020年,荃信生物与华东医药达成合作,后者作为该产品上市许可持有人负责中国大陆区域的商业化。(记者 何凡)
2025-03-26 17:08
【华东医药:全资子公司获得药物临床试验批准通知书】3月26日电,华东医药(000963.SZ)公告称,公司全资子公司中美华东收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,由中美华东申报的HDM3019临床试验申请获得批准。HDM3019是靶向OX40L和TNFα的双特异性抗体,用于治疗类风湿关节炎。该药物已在美国完成Ⅰa期研究,展现出良好的安全性和耐受性。本次临床试验获批将进一步提升公司在自身免疫治疗领域的核心竞争力。
2025-03-13 11:25
【美国ITC发布对水润皮肤磨削系统及其组件的337部分终裁】3月13日电,据中国贸易救济信息网,3月12日,美国国际贸易委员会(ITC)发布公告称,对特定水润皮肤磨削系统及其组件(Certain Hydrodermabrasion Systems and Components Thereof,调查编码:337-TA-1416)作出337部分终裁:对本案行政法官于2025年2月19日作出的初裁(No.15)不予复审,即基于申请方撤回,终止对列名被告的调查。 2024年9月5日,美国国际贸易委员会(ITC)投票决定对特定水润皮肤磨削系统及其组件(Certain Hydrodermabrasion Systems and Components Thereof)启动337调查(调查编码:337-TA-1416)。 2024年8月6日,美国HydraFacial LLC f/k/a Edge Systems LLC of Long Beach, CA向美国ITC提出337立案调查申请,主张对美出口、在美进口和在美销售的该产品违反了美国337条款(侵权美国注册专利号11,865,287、9,550,052),请求美国ITC发布有限排除令、禁止令。 美国Sinclair Pharma U.S. Inc. of Irvine, CA、英国Sinclair Pharma Limited of United Kingdom、中国浙江Huadong Medicine Co., Ltd. of China华东医药股份有限公司、爱尔兰EMA Aesthetics, Ltd. of Ireland、美国Aesthetics Management Partners of Cordova, TN、美国Advanced Aesthetics Services LLC of Miami, FL、美国Advanced Aesthetics Services LLC of Hampton Bays, NY、韩国H.R. Meditech of Korea为列名被告。
2025-03-05 18:22
【华东医药:全资子公司收到医疗器械注册申请受理通知书】3月5日电,华东医药(000963.SZ)公告称,公司全资子公司Viora Ltd.于2025年3月5日收到国家药品监督管理局签发的《受理通知书》,其申报的三类医疗器械光学射频治疗仪V30注册申请获得受理。V30是Viora开发的医美多功能操作平台,可搭载多种治疗手柄,提供面部及身体的全面解决方案。本次V30顺利完成注册受理,是其在中国注册进程中的又一个重大里程碑,公司后续将继续积极推进这款产品在中国的注册工作。
2025-03-03 17:18
【华东医药:全资子公司获得HDM1005注射液临床试验批准通知书】3月3日电,华东医药(000963.SZ)公告称,公司全资子公司中美华东收到NMPA核准签发的《药物临床试验批准通知书》,由中美华东申报的HDM1005注射液临床试验申请获得批准。HDM1005注射液是多肽类人GLP-1受体和GIP受体的双靶点长效激动剂,用于射血分数保留心力衰竭(HFpEF)合并肥胖或超重成人患者的治疗。这是该款产品研发进程中的重要进展,将进一步提升公司在内分泌治疗领域的核心竞争力。
2025-02-25 09:37
【华东医药:GLP-1/GIP双靶点长效激动剂HDM1005注射液新适应症中国IND获得批准】华东医药股份有限公司宣布,公司全资子公司杭州中美华东制药有限公司收到国家药品监督管理局(NMPA)核准签发的《药物临床试验批准通知书》,由中美华东申报的HDM1005注射液临床试验申请获得批准,适应症为用于阻塞性睡眠呼吸暂停(OSA)合并肥胖或超重成人患者的治疗。
2025-02-24 16:57
【华东医药:全资子公司HDM1005注射液临床试验申请获批】华东医药公告,全资子公司杭州中美华东制药有限公司收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,由中美华东申报的HDM1005注射液临床试验申请获得批准。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 从迷糊到高手:解锁股市盈利的五大密钥
- KDJ指标实战精髓:精准捕捉短线行情的秘诀
- 保持积极心态,掌握成功赚钱的十七条金律
- 炒股赚钱之道:控制损失是首要任务
- 揭秘股市神秘信号:底部岛形反转的买入良机
- 股民稳定盈利的智慧之路:掌握三大基石
- 极端行情下的智慧选股:策略与实践
- MACD指标的实战应用:精准捕捉进场时机与强势股信号
- 深入解析股价与均线背离:洞察市场趋势的钥匙
- KDJ指标深度解析:探索被忽视的背离与高级应用策略
- 期货市场开户管理:规范流程,强化监管,确保市场稳健运行
- 揭秘股市迷雾:低位放量上涨出逃形态的深度剖析
- 股市交易中的七大致命错误及应对策略
- MACD指标的实战精髓:精准捕捉买入时机
- 期权交易盈亏解析:掌握盈亏计算方法,洞悉期权市场脉搏
- 揭秘股市风云:深度解析龙虎榜的奥秘
- 仓位管理的艺术:八大法则引领稳健投资之旅
- 炒股智慧:构建稳健的投资体系,实现复利增长
- 揭秘龙头战法之跌停龙头抢筹策略
- 市场风云:掌握被动投资法,驾驭股市震荡
当前版本:V3.0

 VIP复盘网
VIP复盘网
