
扫码报名
阿尔茨海默病:作为一种神经系统退行性疾病,阿尔茨海默病全球仅两款药物,我国目前每年在阿尔茨海默病上支出的费用高达1677亿美元,预计到2030年增加约2倍
- 板块介绍
- 板块资讯
- 强势股票
1、板块介绍
阿尔茨海默病(Alzheimer's disease,AD)作为最常见的痴呆类型,是一种起病隐匿、进行性发展的神经退行性疾病。临床上以不断进展的记忆障碍、全面智能减退、个性改变以及精神行为异常为主要表现。根据患者病情,AD通常分为: 临床前期; 轻度认知障碍(Mild Cognitive lmpairment,MCI); 轻度、中度AD、及重度AD。其中MCI是干预AD的重要阶段,可能延缓AD的发生。
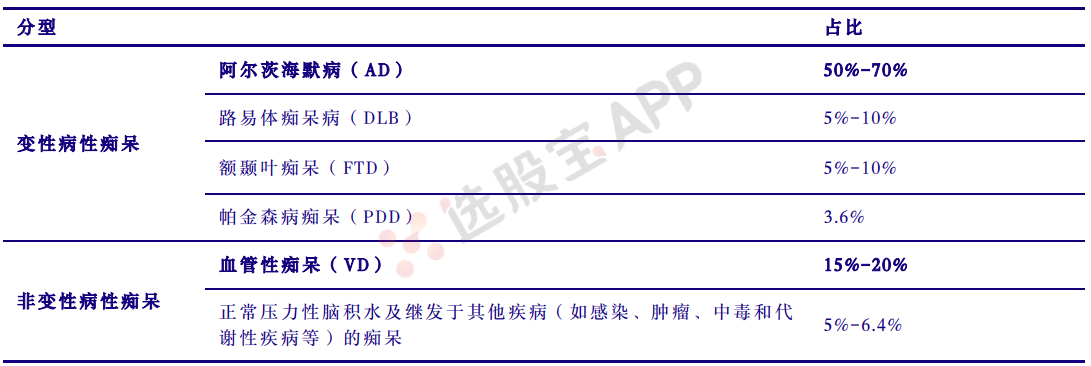
在主要痴呆症分型中,阿尔茨海默病(AD)为主要变性病性痴呆(占比 50%-70%),血管性痴呆(VD)为主要非变性病性痴呆(占比 15%-20%)。从疾病特征差异来看,阿尔茨海默病一般多见于女性,病程持续进行,自觉症状较少且伴随全面性痴呆、人格崩溃、精神行为异常,CR/MRI 下可见脑萎缩,PET/SPECT 可见颞、顶叶对称性血流低下。
近年来阿尔茨海默病(AD)领域发展迅速,比如AD新型靶向治疗药物的批准上市,以及血浆生物标志物在AD临床诊断研究中的应用等。在2023年阿尔茨海默病协会国际会议上,美国梅奥诊所的Clifford Jack医生领衔的美国国家老龄化研究所-阿尔茨海默病协会(NIA-AA)的科学家团队,提交了《NIA-AA阿尔茨海默病临床诊断指南修订版》的草案。
本次NIA-AA修订版指南强调从生物学角度重新定义AD,这将推动未来大规模地从生物学角度来诊断AD,比如通过脑脊液检测AD生物标志物,或者通过脑成像技术检测大脑中的斑块和缠结实现AD的病理学诊断。生物标志物检测新技术促进AD的病理诊断。以往阿尔茨海默病只能在患者逝世后,通过脑部显微镜检查发现斑块和缠结物才可以完全确诊。现在的生物标志物检测技术能够在患者在世时就检出斑块和缠结的存在,尽早明确AD的病理诊断。
目前生物标志物检测技术主要包括特定类型的脑部PET扫描,以及可以测量血浆和脑脊液中的淀粉样蛋白和tau蛋白的相关检查。新型靶向治疗药物有望减缓AD的疾病进展。对于开发能够阻止或延缓AD疾病进展的治疗方法,专家们抱有谨慎但乐观的态度。现在在研的药物治疗策略主要包括以β-淀粉样蛋白斑块为靶向的策略,阻止tau蛋白形成纤维缠结的策略,减少中枢炎症的策略以及激素替代治疗策略等,目前已取得一定突破的主要是以β-淀粉样蛋白斑块为靶点的治疗策略。
诊断:分子影像诊断引领,体液标志物检测研发加速。目前AD检测方法包括神经影像学检查、神经心理测评、体液标志物等。先通医药的氟[18F]贝他苯注射液为国内首款获批的Aβ-PET显像剂。东诚药业的Tau蛋白正电子摄影示踪剂正在进行III期临床。国内在研AD诊断试剂在Tau、Aβ靶点均有布局。
治疗:聚焦Aβ靶点,多款新药海外获批上市。近年申报的AD药物以靶向Aβ为主,如礼来制药2023年10月申报上市的Donanemab和卫材药业于2022年底申报的仑卡奈单抗(商品名:乐意保)。仑卡奈单抗在今年10月落地海南博鳌乐城国际医疗旅游先行区。国内在研治疗用AD药物大部分为引进产品,近年进入III期的AD治疗药物同样多聚焦于Aβ靶点。
2024-12-18 09:29
礼来阿尔茨海默病疗法记能达®(多奈单抗注射液)在中国获批
今天,中国国家药品监督管理局批准礼来公司(纽约证券交易所代码:LLY)的阿尔茨海默病疗法, 记能达®(多奈单抗注射液,每四周一次静脉输注)用于治疗成人因阿尔茨海默病引起的轻度认知功能障碍和阿尔茨海默病轻度痴呆。记能达®是唯一一个有证据支持在清除淀粉样蛋白斑块后可停药的靶向淀粉样蛋白的疗法,这可以通过减少输液次数和治疗成本帮助患者降低治疗负担。继美国、日本、英国之后,中国是批准记能达®上市的又一主要市场。(礼来Lilly微信公众号)
2024-11-25 22:38
木薯科学(SAVA)下跌85%,创该公司美国IPO以来最大盘中跌幅。 该公司ReThin-ALZ第三阶段临床试验结果表明,Simufilam没能在降低老年痴呆症轻度至中度受试病患的认知或功能下降方面实现联合终点
2024-11-15 00:03
欧洲药品管理局推荐将Leqembi用于治疗早期阿尔茨海默症
欧洲药品管理局(EMA)经过重新评估自身的初步意见,决定推荐将Leqembi用于治疗早期阿尔茨海默症。 EMA下辖人用药委员会建议,授予日本卫材和渤健联合开发的Leqembi市场销售资质,用于治疗阿尔茨海默症造成的轻度认知损伤或中度痴呆。 本轮再评估认为,在一个严格限制的受试病患样本群体中,Leqembi利大于弊。 渤健(BIIB)涨幅扩大至超过5.15%,报175.86美元。
2024-10-30 00:02
礼来制药:一项研究的初步结果显示,小幅调整阿尔茨海默症药品Kisunla的剂量,降低了受试病患发生脑肿胀副作用的风险
2024-08-29 15:51
通化金马:收到琥珀八氢氨吖啶片上市申请登记受理通知书
通化金马公告,近日,公司收到国家药品监督管理局签发的琥珀八氢氨吖啶片上市申请的《受理通知书》。琥珀八氢氨吖啶片是一种新型的、强效、作用机制明确的胆碱酯酶抑制剂,是拥有完全自主知识产权、新化学分子结构、境内外均未上市的化学 1 类新药。用于轻、中度阿尔茨海默病(AD)的治疗。与已上市抗AD药物相比,患者获益突出且不增加安全性风险,获益远大于风险。琥珀八氢吖啶片有望成为AD治疗领域安全,有效的首选药物。公司将全力推进该药在中国的注册上市。
2024-08-29 14:59
通化金马回应口服阿尔茨海默病药申报上市:如果走绿色通道,最快半年可上市
8月29日,据国家药监局药品审评中心官网,通化金马的琥珀八氢氨吖啶片申报上市,这是一款潜在的国产口服阿尔茨海默病(AD)新药。此前,通化金马曾表示,该药物的原料药已经上市申请,后续会提交片剂上市申请。对此,记者以投资者身份联系了通化金马的投资者关系部门,相关人士介绍,此次上市申请获受理的正是片剂。原料药和片剂均获批后,琥珀八氢氨吖啶片可以上市吗?该人士称,“要等国家药监局审核之后,也得过一段时间,要审批资料之类的。”对于该药上市时间,该人士称,如果(实现走)绿色通道的话,最快也是半年。 (21财经)
2024-07-31 05:03
卫材和渤健BIIB研究结果显示:那些使用治疗阿尔茨海默症的药品Leqembi的病患能获得超过三年的好处。 这表明,老年痴呆症患者需要长期使用这种疗法
2024-07-28 10:00
新发现:打了这种疫苗,老年痴呆症发生延缓了
《自然》杂志最新刊登研究发现,接种带状疱疹疫苗与痴呆症发生率的降低相关联。这一结果若在未来的临床试验中得到证实,带状疱疹疫苗或许将成为一种既经济又有效用以预防或延缓痴呆症的手段!
2024-07-03 08:06
全球首批!FDA批准礼来阿尔茨海默病疗法
亚群分析显示,donanemab能显著减缓患者的认知与功能下降达60%,特别是早期患者和75岁以下患者受益显著。
2024-07-03 01:47
礼来延缓阿尔茨海默病的药物获得美国批准
礼来公司表示,美国食品和药物管理局(FDA)已批准Kisunla用于有阿尔茨海默病早期症状的成人患者。 6个月的疗程费用为12,522美元,12个月的费用为32,000美元,18个月的费用为48,696美元。
2024-06-29 04:30
老年痴呆症概念股木薯科学股价盘中一度腰斩
木薯科学(SAVA)收跌34.83%,报12.35美元,北京时间02:00之前跌幅一度超过53.61%。 拜登政府盯上该公司一名前顾问,木薯科学回应称,该顾问未曾参与该公司Simufilam的第三阶段临床试验,该药品是木薯科学用于治疗阿尔茨海默症的主打候选药。
2024-06-11 22:50
美股老年痴呆疗法概念股普跌
Axsome Therapeutics美股早盘跌约6.7%,Longeveron跌6.6%,PRTA跌2.8%,Annovis Bio跌2.4%,INume Bio跌0.9%,木薯科学SAVA跌1.1%,渤健则涨0.2%,礼来制药涨0.38%——美国食品药品管理局(FDA)一个委员会6月10日全票支持其阿尔茨海默症疗法利大于弊。
2024-05-10 17:38
诺唯赞:全资子公司诺唯赞医疗与上药康德乐就公司阿尔茨海默病(AD)血检产品等业务合作事宜签订《合作协议》
2024-04-30 00:19
临床阶段制药公司Annovis Bio Inc.(ANVS)一度跌约70%,刷新2020年10月份以来盘中低点至5.23美元,该公司针对轻度至中度阿尔茨海默症(AD)患者疗法的2/3阶段临床试验结果让人感到失望——达到一个主要终点、但没能实现另外一个主要终点
2024-04-14 15:38
诺唯赞:全资子公司诺唯赞医疗与毓舫医疗签订战略合作协议,围绕诺唯赞医疗阿尔茨海默病血液检测产品加强合作
| ID | 股票名称 | 涨幅% | 现价 | 换手率% | 总市值 | 炒作逻辑 |
|---|

 VIP复盘网
VIP复盘网
