
扫码报名
猴痘概念:2022年5月,猴痘疫情在英国、西班牙、美国等多国蔓延,相关检测和治疗公司迎来发展机遇
- 板块介绍
- 板块资讯
- 强势股票
1、板块介绍
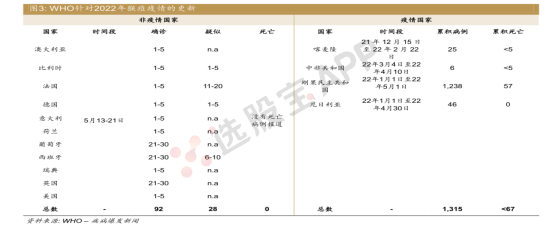
2022年5月21日,世卫组织更新猴痘已蔓延至12个非疫情国家,当中有92个实验室确诊病例(如葡萄牙、西班牙和英国报告21-30例确诊病例)和28个疑似病例。尽管这些国家没有死亡报告,但世卫组织警告说,随着在非流行国家扩大监测范围,将确认更多病例,并发出警报,因为这种致命病毒很少传播到病例非常罕见的地区。
猴痘病毒是一种包膜双链DNA病毒,属于痘病毒科正痘病毒属。在中非(~10% 死亡率)和西非进化枝(~1% 死亡率)发现了两个猴痘病毒遗传进化枝,其中前者更为严重。值得注意的是,猴痘基因组的双链性质意味着它比 RNA 病毒 SARS-CoV-2 更稳定,并且由于其具有基因修复机制而不易发生快速突变。
猴痘是一种病毒性人畜共患病,能够人传人,如松鼠、大鼠和猴。人与人之间的传播主要是由于与感染者的密切接触。病毒通过破损的皮肤(即使不可见)或粘膜(眼睛、鼻子或嘴巴)进入人体。通过呼吸道传播也是可能的,但需要更长的接触时间。R值是指一名感染者可以传播该疾病的人数(猴痘为2.13,SARS-CoV-2为12)。
在人类中,猴痘的症状与天花的症状相似但较轻。猴痘病始于发烧、头痛、肌肉酸痛、淋巴结肿大和疲惫。在最初发病后大约1-3天后,患者出现皮疹,通常从面部开始,然后扩散到身体的其他部位;病变从斑疹、丘疹和水疱发展为结痂,最后在2-4周内痊愈。
从历史上看,猴痘主要在非洲传播,90年代刚果盆地的农村、热带雨林地区有报道。 2017年,尼日利亚发生大规模疫情(即确诊病例超过200例,病死率约3%)。此后,美国(2003 年)、新加坡(2019 年)和英国(2021 年)相继报告了输入病例,并且病例持续报告到今天。
2、猴痘检测、预防和治疗
猴痘病毒是一种包膜双链 DNA 病毒,和天花病毒同属正痘病毒,正痘病毒属还包括痘苗病毒、牛痘病毒和其他几种与动物有关的痘病毒。猴痘传染性有限(R0<1),症状一般可自愈,病死率在1%-10%;而天花传染性较强(R0=4),症状极为迅猛凶险,病死率高达30%。由于正痘病毒免疫反应能够提供交叉保护,因此主要基于牛痘病毒设计天花和猴痘疫苗。自 1980年WHO宣布消灭天花后,人们不再接种天花疫苗,但天花疫苗仍然对猴痘产生85%的交叉免疫保护。
美国已批准的两款疫苗对猴痘有预防作用。1)JYNNEOS,2019 年 9月获 FDA 批准上市用于预防天花和猴痘,丹麦 Bavarian Nordic 公司研发,改良减毒非复制型牛痘病毒,两剂次接种。2)ACAM2000,2007 年获 FDA 批准上市用于预防天花,但对猴痘也有 85%的交叉免疫保护,英国 Acambis 公司研发,牛痘活病毒,单剂次接种。
国内主要是国药集团中国生物有一款天花疫苗储备。我国 1981 年宣布停止接种天花疫苗,目前主要是国药集团中国生物旗下北京所每年生产若干数量的“天坛株”天花疫苗作为储备。但天花疫苗对猴痘仍有85%的交叉保护。
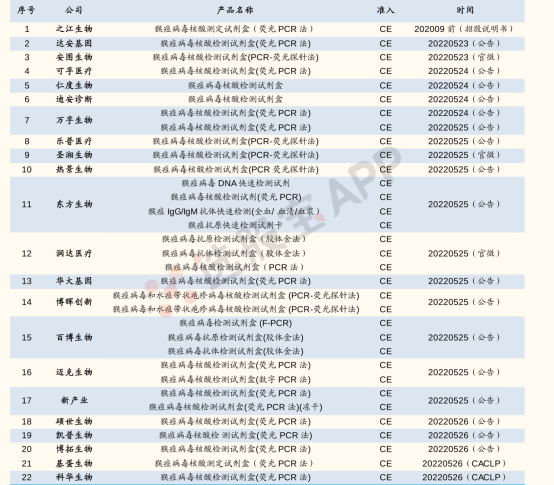
另外,国内多家企业已有猴痘检测试剂上市/储备。猴痘的临床症状与其他皮疹疾病如天花、水痘、麻疹、疥疮、梅毒等初期症状非常相似,只能由实验室确诊,需要在专业实验室中通过一些检测方法测定病毒,可以使用血液和血清样本 。目前国内已有多家企业上市或者储备猴痘检测试剂。
目前尚无针对猴痘的特效药物,抗病毒药物、牛痘免疫球蛋白可以被使用。1)特考韦瑞(tecovirimat):2018年FDA批准首款治疗天花的TPOXX的口服剂型(SIGA Technologies研发)。2022 年1月,EMA 批准上市用于治疗天花、猴痘、牛痘等。2022年5月19日FDA 批准了TPOXX的静脉注射剂,用于无法吞咽胶囊的患者。该药的抗病毒机制为通过与病毒基因结合,阻止病毒从细胞内释放。2)西多福韦(Cidofovir)和布林西多福韦(Brincidofovir):两者都已在体外和动物研究中证明了对猴痘病毒的活性,其中布林西多福韦 2021年被FDA 批准上市用于治疗天花,但尚未进行猴痘的临床试验或者猴痘病例治疗。3)牛痘免疫球蛋白:目前尚未证实猴痘免疫球蛋白对猴痘感染者的有效证据,但紧急情况下可以使用。4)其他广谱抗DNA病毒药物。如Acyclovir(阿昔洛韦)、Valacyclovir(伐昔洛韦)、更昔洛韦(ganciclovir)、泛昔洛韦(famciclovir)、喷昔洛韦(penciclovir)、Idoxuridine(碘苷)、Vidarabine(阿糖腺苷)、Lamivudine(拉米夫定)等可以直接或者间接抑制DNA复制从而达到抗病毒效果。干扰素、Thymosinα1(胸腺肽α1)等具有抗病毒、免疫调节等作用。
2024-12-12 17:26
我国自主知识产权猴痘疫苗获批临床
12月10日,由中国生物北京生物制品研究所与中国疾病预防控制中心病毒病预防控制所合作研发的猴痘疫苗,获得国家药品监督管理局签发的药物临床试验批准通知书,注册分类为1.2类创新型疫苗。该疫苗是中国科学家自主研发的具有完全自主知识产权的创新型疫苗,有望在我国预防和控制猴痘病毒导致的疾病方面发挥重要作用。(澎湃)
2024-11-07 12:58
英国猴痘病例增至4例,非洲以外首现集群感染
英国卫生安全局6日通报,在上周确诊首名猴痘病毒新毒株感染者的家庭接触者中又发现一名感染者,至此,这一新毒株在英国的感染病例增至4例,首次在非洲以外地区造成集群感染。(央视新闻)
2024-09-09 20:34
宁德时代连续大手笔布局光伏产业,行业落后产能持续出清,基本面拐点有望加速到来;我国首款猴痘疫苗进入临床阶段,产业链有望转向响应预期需求 | 9月10日早知道
随着终端需求持续释放,库存水平不断下降,光伏基本面有望逐步企稳。
2024-09-03 16:20
我国首次鉴定出猴痘新谱系,专家:本土大流行可能性低
近日,我国科研团队在国际医学杂志《自然·通讯》上发表最新研究:首次鉴定出猴痘C.1.1新谱系。北京佑安医院感染综合科主任医师李侗曾表示,C.1.1谱系的致病率、传染性未发生明显变化,猴痘在我国本土大流行可能性很低。此外,近期亚洲出现首例猴痘Ib变异株病例。与其他猴痘病毒相比,Ib变异株可通过呼吸道传播、有妇女和儿童感染病例等新特点引发关注。对此,李侗曾表示,临床中,90%以上的猴痘病例是通过皮肤密切接触而感染的,特别是在性行为接触中感染。虽然理论上存在呼吸道传播方式,但在实际传染性相对较弱。(北京日报)
2024-08-30 15:56
一款天花疫苗获美药管局批准用于预防猴痘感染
美国新兴生物科技公司29日发布公报说,美国食品和药物管理局已正式批准扩大该公司生产的一款天花疫苗的适应症范围,允许这款疫苗用于帮助高风险人群预防猴痘病毒感染。公报说,这项审批是基于已获得的人体安全性数据和动物实验数据。动物实验数据显示,这款名为ACAM2000的天花疫苗可有效预防猴痘病毒感染。新兴生物科技公司近日宣布,将向猴痘疫情最严重的刚果(金)以及布隆迪、肯尼亚、卢旺达和乌干达等其他受影响的国家捐赠5万剂ACAM2000疫苗。(新华社)
2024-08-27 17:05
万泰生物在互动平台表示,猴痘核酸试剂已在规划中,公司将根据市场需求及商业价值进行综合判断是否启动临床
2024-08-27 09:03
猴痘概念:世卫组织启动全球战略准备,一盘后大涨的美股已增加产能,取得CE认证企业有望受益
随着猴痘疫情的持续蔓延,全球对防疫产品的需求不断增长。
2024-08-26 19:51
世卫组织启动全球战略准备和应对计划,遏制猴痘疫情蔓延
世界卫生组织8月26日启动了一项全球战略准备和应对计划,以通过全球、地区和国家的协调努力,阻止猴痘在人际间的传播。据介绍,该计划涵盖2024年9月至2025年2月的6个月,预计需要1.35亿美元的应对资金。为满足实施该计划的需要,世卫组织将发出筹资呼吁。(央视新闻)
2024-08-22 18:25
泰国确诊亚洲首例猴痘新毒株病例(彭博)
2024-08-19 18:33
合富中国:公司有向部分医院客户销售猴痘病毒核酸检测试剂盒产品,但猴痘病毒核酸检测相关产品对公司业绩占比较小,对公司营业收入未产生实质或重大影响
2024-08-19 16:26
美股盘前,猴痘概念股涨幅扩大,GeoVax Labs涨超60%,Chimerix涨近18%
2024-08-19 15:59
达安基因:取得猴痘病毒核酸检测试剂盒注册证
达安基因公告,近日,公司取得国家药品监督管理局颁发的医疗器械注册证一个。医疗器械名称:猴痘病毒核酸检测试剂盒(荧光 PCR 法),注册证编号:国械注准20243401527。有效期自批准之日起至2029年8月17日。
2024-08-09 15:00
非洲疾控中心呼吁采取紧急措施控制猴痘传播
当地时间8月8日,非洲疾病控制和预防中心呼吁非洲各国采取紧急行动,避免猴痘疫情在非洲大陆持续蔓延。8日,非洲疾控中心主任让·卡塞亚在线上会议中说,目前非洲至少有16个国家受到猴痘影响;与2023年同期相比,非洲今年报告的猴痘病例增加了160%。他说,各国必须采取强有力的行动,遏制目前在非洲蔓延的猴痘疫情。(央视新闻)
2024-08-08 14:40
世卫组织决定就猴痘疫情召集紧急委员会会议
当地时间7日,世界卫生组织总干事谭德塞在瑞士日内瓦举行的记者会上表示,鉴于猴痘病毒在刚果(金)境外传播,及其可能在非洲内外进一步扩散的潜在风险,他已决定根据《国际卫生条例》召集紧急委员会尽快召开会议,以评估此次猴痘疫情是否构成“国际关注的突发公共卫生事件”。(中国新闻网)
2023-10-15 15:57
中疾控周报:猴痘病毒在北京本土传播得到显著抑制
近日,中国疾控中心周报发布《生命周期监测:近期流行猴痘病毒84个基因组的遗传特征——北京市,2023年》:猴痘病毒在北京本土传播得到显著抑制,所有猴痘病毒基因组与目前在东亚和东南亚地区流行的基因组具有高度同源性。(北京日报)
| ID | 股票名称 | 涨幅% | 现价 | 换手率% | 总市值 | 炒作逻辑 |
|---|



 VIP复盘网
VIP复盘网
