
扫码关注公众号
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
汇宇制药
688553 |
-3.46%
|
最新:16.48
开盘:16.9 昨收:17.07 |
开盘%:-1%
振幅%:4.98% 换手%:2.72% |
最高:17.2
最低:16.35 量比:1.21 |
总市值:70 亿
流通值:51 亿 成交额:3 亿 |
- 基本信息
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- Deepseek分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
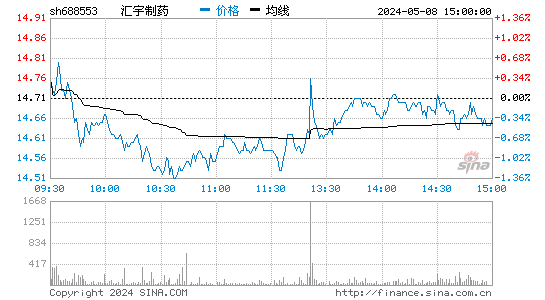
- 分时图
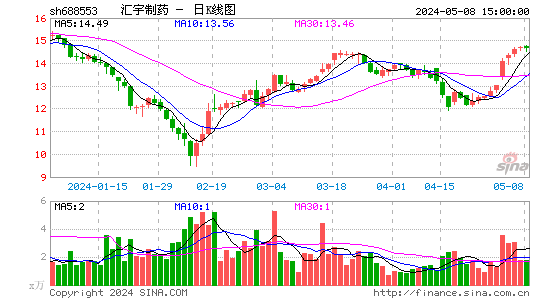
- 日K图
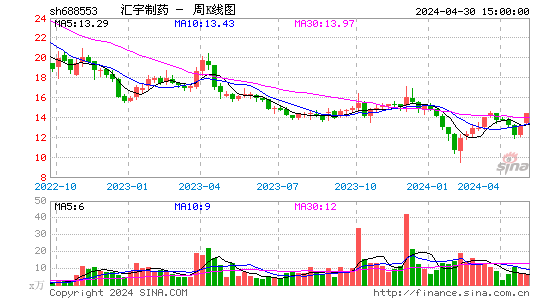
- 周K图
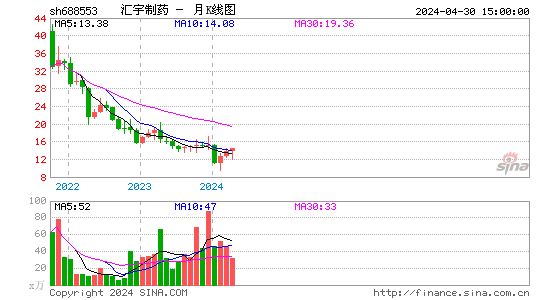
- 月K图
汇宇制药-W股票概况
全面解析汇宇制药-W的投资价值与行业地位
公司概况
主营业务:汇宇制药-W的主营业务为抗肿瘤和注射剂药物的研发、生产和销售,主要产品包括原料药、抗肿瘤注射剂、肿瘤辅助用药和造影剂等。
行业地位:作为注射用阿扎胞苷产品的国内首仿企业之一,汇宇制药在化学制药行业,尤其是抗肿瘤药物领域具有较高的知名度和市场占有率。
产品与技术
产品线:汇宇制药拥有丰富的产品线,包括多个中选国家集采的抗肿瘤药物,如奥沙利铂注射液、多西他赛注射液等。
技术优势:公司在产品研发方面具有明显的技术优势,参与了多项行业标准的制定,并拥有多项核心专利技术。
财务表现
营收与利润:近年来,汇宇制药的营业收入和净利润均保持快速增长。尽管在某些季度受到研发投入增加等因素的影响,净利润出现波动,但整体财务表现稳健。
盈利能力:公司的毛利率和净利率均高于行业平均水平,显示出较强的盈利能力。
市场前景与投资潜力
行业前景:随着国内化学制药行业的快速发展和抗肿瘤药物需求的不断增长,汇宇制药的市场前景广阔。
投资潜力:作为抗肿瘤药物领域的佼佼者,汇宇制药具有较高的投资潜力。然而,投资者也需关注行业竞争加剧、政策变化等潜在风险。
总结
汇宇制药-W作为化学制药行业的佼佼者,在抗肿瘤药物领域具有显著优势。公司拥有丰富的产品线和技术优势,财务表现稳健,市场前景广阔。然而,投资者在关注其投资价值的同时,也需警惕潜在风险。
2025-03-31 19:23
【汇宇制药:股东黄乾益拟减持不超公司总股本的3%】《科创板日报》31日讯,汇宇制药(688553.SH)公告称,持股5%以上股东黄乾益因自身资金需求,拟通过集中竞价或大宗交易的方式减持公司股份不超过1270.8万股,合计减持股份比例不超过公司股份总数的3%。减持期间为自本公告披露之日起15个交易日后的3个月内。
2025-03-11 17:43
汇宇制药:注射用塞替派获得药品注册证书
2025-02-24 17:41
汇宇制药:收到土库曼斯坦药品管理局、西班牙药品和医疗器械管理局、意大利卫生部和英国药品和健康产品管理局分别核准签发的公司产品注射用培美曲塞二钠、注射用赛替派、注射用环磷酰胺、注射用帕瑞昔布钠的上市许可。
2025-02-10 17:20
【汇宇制药:公司产品获得境外上市许可】《科创板日报》10日讯,汇宇制药公告称,公司子公司Seacross Pharma (Europe) Ltd.及Seacross Pharmaceuticals Ltd.近期收到荷兰、哥斯达黎加、秘鲁、巴基斯坦等国家核准签发的公司产品注射用环磷酰胺、盐酸伊立替康注射液、普乐沙福注射液、氟维司群注射液的上市许可。这些许可将有利于公司在国际市场产品管线的丰富,提升市场品牌形象,持续拓展国际业务的广度和深度,为国际市场的可持续发展奠定基础。
2025-02-10 17:20
汇宇制药:近期收到荷兰健康产品监管局、哥斯达黎加卫生部、秘鲁药品和药物管理局、巴基斯坦药品监管局和卫生部分别核准签发的公司产品注射用环磷酰胺、盐酸伊立替康注射液、普乐沙福注射液、氟维司群注射液的上市许可
2025-01-22 11:46
【汇宇制药成立新公司 含药品进出口业务】企查查APP显示,近日,四川汇辰昕药业有限公司成立,法定代表人为袁永越,注册资本100万元,经营范围包含:药品批发;药品进出口;医学研究和试验发展;企业管理咨询等。企查查股权穿透显示,该公司由汇宇制药全资持股。
2025-01-21 16:49
汇宇制药:亚叶酸钙注射液获得药品注册证书
2025-01-10 18:11
【汇宇制药:全资子公司获法国、埃及药品上市许可】汇宇制药公告,全资子公司Seacross Pharmaceuticals Ltd.近日收到法国国家药品和保健品安全局、埃及药品管理局核准签发的公司产品注射用替考拉宁、多西他赛注射液的上市许可。
2025-01-10 16:42
汇宇制药:注射用替考拉宁、多西他赛注射液分别获得法国、埃及上市许可。
2024-12-27 16:23
汇宇制药:HY-2003I期临床试验首例受试者给药
2024-12-23 18:08
汇宇制药:注射用环磷酰胺获得美国FDA批准
2024-12-20 16:11
汇宇制药:化学创新药HYP-6589片I期临床试验首例受试者给药
2024-12-18 16:18
汇宇制药:注射用唑来膦酸浓溶液、丙戊酸钠注射用浓溶液、注射用环磷酰胺、注射用伏立康唑分别获得埃及、西班牙、葡萄牙、德国上市许可
2024-12-10 17:01
汇宇制药:注射用环磷酰胺获得爱尔兰上市许可。
2024-11-27 16:56
【汇宇制药:注射用氨磷汀、吗啉硝唑氯化钠注射液获得药品注册证书】11月27日电,汇宇制药公告称,公司及其全资子公司汇宇海玥近日收到国家药品监督管理局核准签发的《药品注册证书》,包括注射用氨磷汀和吗啉硝唑氯化钠注射液两种药品。注射用氨磷汀的原研未在国内上市,目前国内有5家企业持有该药品批件,其中仅开封明仁和汇宇海玥通过或视同通过仿制药质量和疗效一致性评价。吗啉硝唑氯化钠注射液的原研是江苏豪森药业,公司是国内首家仿制药企业,也是首家视同通过仿制药质量和疗效一致性评价的企业。两种药品的注册分类分别为化学药品3类和4类,批准后视同通过仿制药质量和疗效一致性评价。公司已开展产品上市销售的前期准备工作,但未来能否产生较大收入具有较大不确定性。
2024-11-27 16:55
汇宇制药:注射用氨磷汀、吗啉硝唑氯化钠注射液获得药品注册证书
2024-11-26 16:13
汇宇制药:HY-2003获得药物临床试验批准通知书
2024-11-25 16:26
汇宇制药:注射用伏立康唑、氟维司群注射液获得英国上市许可。
2024-10-18 16:52
汇宇制药:公司员工持股平台内江衡策、内江盛煜自愿承诺,自2024年10月28日起未来6个月内不减持公司股份。内江衡策、内江盛煜目前合计持股比例为4.35%
2024-10-09 16:20
【汇宇制药:子公司产品获埃及、荷兰、葡萄牙、西班牙上市许可】《科创板日报》9日讯,汇宇制药公告,子公司Seacross Pharmaceuticals Ltd.和Seacross Pharma (Europe) Ltd.近日分别收到埃及、荷兰、葡萄牙、西班牙相关机构签发的公司产品盐酸多柔比星注射液、丙戊酸钠注射用浓溶液、唑来膦酸注射液的上市许可。这些产品分别用于治疗多种癌症、癫痫以及骨质疏松症等疾病。公司表示,此次获得上市许可有利于丰富公司在国际市场的产品管线,提升品牌形象,为国际市场的可持续发展进一步夯实基础。但产品未来能否产生较大收入存在不确定性。
2024-09-20 15:45
【汇宇制药:子公司注射用HY07121获得药物临床试验批准通知书】9月20日电,汇宇制药公告,全资子公司汇宇海玥收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,生物创新药注射用HY07121(项目研发代号为“HY-0007”)用于治疗晚期实体瘤的临床试验获得批准。注射用HY07121是公司全资子公司汇宇海玥自主研发的抗PD-1、抗TIGIT、IL-15/IL-15Rα双抗融合蛋白,其注册分类为1类创新型治疗用生物制品。国内外尚无同类产品获批上市。
2024-08-27 17:13
汇宇制药:普乐沙福注射液、注射用阿扎胞苷、注射用塞替派分别获得以色列、埃及、北爱尔兰上市许可。注射用环磷酰胺获得国家药品监督管理局核准签发的《药品注册证书》
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 老股民的股海沉浮与智慧成长
- 掌握短线操作的三大关键技巧
- DMI与CDP:股市投资的黄金组合指标
- 解锁股票上涨之谜:洞悉个股上扬的核心特征
- 开盘后30分钟:洞悉股市走势的关键时刻
- 揭秘移动平均线选股策略:精准捕捉买卖时机
- 揭秘庄股突破:深度解析庄家操盘策略与散户应对之道
- 四步策略,打造短线炒股高手之路
- 股市破位抄底的智慧与策略
- 解套术:股市被套后的应对策略
- 揭秘股市赢家秘籍:深度解析高抛低吸的成功之道
- 股票投资:心态、策略与持续学习的三重奏
- 美股高歌猛进,海运板块强势反弹:道指连创新高与OPEC减产预期共舞
- SAR停损指标:散户投资的智慧导航
- 股市逆势盈利策略:五大实战技巧深度剖析
- 掌握股票投资精髓,揭秘成功秘诀
- 趋势操作:选股策略助力跑赢大盘
- 能量潮指标OBV:中短线投资的智慧钥匙
- 手机炒股软件指标下载与使用指南:避坑策略与实战技巧
- 均线实战精髓:深度解析抗拒“骗线”策略
当前版本:V3.0

 VIP复盘网
VIP复盘网
