
扫码关注公众号

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
百利天恒
688506 |
-0.43%
|
最新:296.12
开盘:298 昨收:297.39 |
开盘%:0.21%
振幅%:3.6% 换手%:0.8% |
最高:299.83
最低:289.13 量比:0.96 |
总市值:1187 亿
流通值:305 亿 成交额:1 亿 |
- 基本信息
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
- 分时图
- 日K图
- 周K图
- 月K图
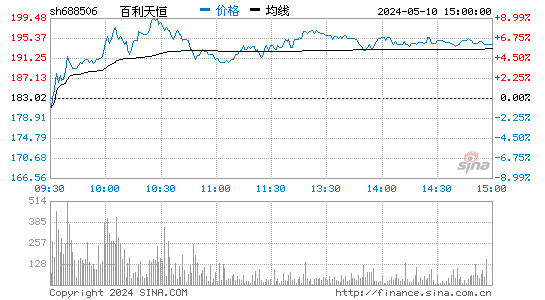
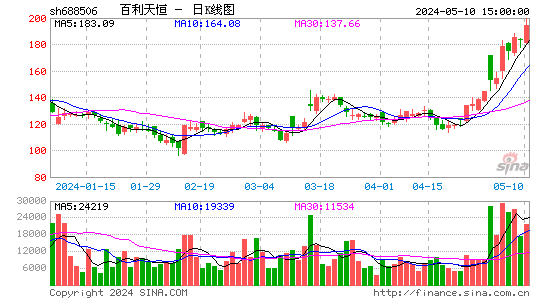
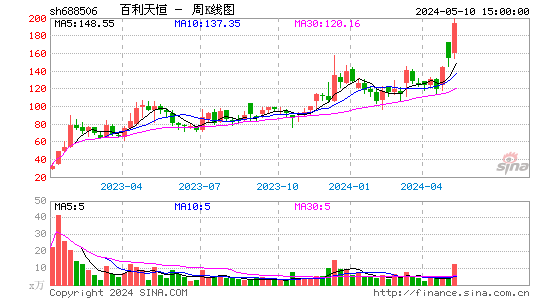
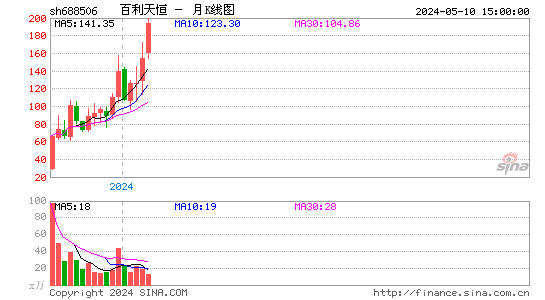
百利天恒-U股票详解
聚焦创新生物药的生物医药企业股票分析
公司概况
百利天恒-U,全称为四川百利天恒药业股份有限公司,成立于2006年8月17日,并于2023年1月6日上市。公司聚焦于全球生物医药前沿领域,致力于解决临床未被满足的需求。
业务与研发能力
百利天恒-U具备包括小分子化学药、大分子生物药及ADC药物的全系列药品研究开发能力。公司拥有从中间体、原料药到制剂的一体化优势,以及覆盖“研发—生产—营销”的完整全生命周期商业化运营能力。
业绩与市场表现
近年来,百利天恒-U的业绩表现亮眼。公司2024年营收预增932%,净利润约36亿元,实现了扭亏为盈。在股市方面,百利天恒-U的股价呈现波动上涨趋势,总市值和流通市值持续增长。
创新药物研发进展
百利天恒-U在创新药物研发方面取得了显著进展。公司自主研发的创新生物药注射用BL-M07D1(HER2-ADC)获得了III期临床试验的批准,这对于公司在乳腺癌治疗领域的布局具有重要意义。
未来展望
展望未来,百利天恒-U将继续聚焦创新生物药的研发,加速推进临床试验进程,争取早日将更多创新药物推向市场,以满足患者的临床需求。
总结:
百利天恒-U作为生物医药领域的佼佼者,凭借强大的研发能力和优异的市场表现,赢得了投资者的广泛关注。未来,随着创新药物的陆续上市,公司有望迎来更加广阔的发展前景。
2025-06-23 17:35
百利天恒:注射用BL-M07D1(HER2 ADC)用于在新辅助治疗后存在浸润癌残留的HER2阳性乳腺癌术后辅助治疗III期临床试验完成首例受试者入组
2025-06-16 07:31
【A股公司赴港上市提速 优质标的获国际长线资金抢筹】6月16日电,今年以来,A股行业龙头企业接连筹备赴港上市,拟构建“A+H”双融资平台。从进展来看,赛力斯、晶澳科技等公司已向中国证监会提交上市备案材料,百利天恒、奥克斯电气等公司已向香港交易所递交上市申请。安永大中华区上市服务主管合伙人何兆烽表示,拟“A+H”两地上市的企业多为细分领域龙头,具备较强稀缺性,可以吸引国际资本持续流入,使市场形成良性循环。未来,预计将有更多大型企业及产业链领军企业登陆港股。国际长线资金愈发热衷于参与优质港股IPO项目。“今年港股IPO的基石投资者认购踊跃。甚至在部分优质项目中,很多机构投资者拿不到基石认购额度,只能通过锚定方式参与。”高盛亚洲(除日本外)股票资本市场主管王亚军表示。(证券日报)
2025-06-07 18:08
【近一周280多只个股获机构调研 中微公司调研机构数最多】6月7日电,近一周机构调研个股数量有280多只,中微公司调研机构数最多。中微公司有212家机构调研,其中包括34家基金公司、61家证券公司、37家私募、7家保险公司等。华测检测、百利天恒、鼎泰高科、中科创达、海南华铁等个股近一周也有逾百家机构调研。其中,百利天恒作为创新药龙头股之一,市值超1200亿元,本周股价创出历史新高,最新收盘价在300元以上,是A股第九高价股。
2025-05-30 20:58
百利天恒:注射用BL-M07D1(HER2 ADC)用于HER2低表达复发或转移性乳腺癌III期临床试验完成首例受试者入组
2025-04-29 17:54
【百利天恒:一季度净亏损5.31亿元】4月29日电,百利天恒(688506.SH)公告称,公司2025年一季度营业收入为6744万元,同比下降98.77%,主要系上年同期确认了大额知识产权授权收入。一季度净亏损5.31亿元,去年同期净利润50.05亿元,主要系营业收入减少和研发费用增加。
2025-04-22 16:25
百利天恒:BL-M11D1(CD33-ADC)联合用药治疗新诊断的急性髓系白血病获得药物临床试验批准通知书
2025-04-15 17:25
百利天恒:BL-B01D1(EGFR×HER3双抗ADC)联合用药治疗多种晚期实体瘤获得4个II期药物临床试验批准通知书
2025-04-08 15:47
百利天恒:BL-B01D1(EGFR×HER3双抗ADC)用于在局部晚期或转移性尿路上皮癌III期临床试验完成首例受试者入组。
2025-03-28 19:52
【百利天恒:2024年净利润37.08亿元 同比扭亏为盈】28日讯,百利天恒(688506.SH)发布2024年年度报告,报告期内公司实现归属于上市公司股东的净利润37.08亿元,较上年同期增加44.88亿元,实现扭亏为盈。公司2024年度利润分配预案为:不派发现金红利,不送股,不以资本公积金转增股本。
2025-03-12 10:43
【百利天恒在成都新设生物科技公司】企查查APP显示,近日,成都诺芯生物科技有限公司成立,法定代表人为朱义,注册资本300万元,经营范围包含:技术服务、技术开发、技术咨询、技术交流、技术转让、技术推广;技术进出口;货物进出口。企查查股权穿透显示,该公司由百利天恒全资持股。
2025-03-09 15:45
【百利天恒:拟定增募资不超39亿元,用于创新药研发项目】百利天恒公告,公司拟向特定对象发行股票募资不超过39亿元,扣除发行费用后将全部用于创新药研发项目。
2025-03-02 16:26
【百利天恒:创新生物药Ⅲ期临床试验完成首例受试者入组】百利天恒公告,公司自主研发的创新生物药注射用BL-B01D1(EGFR×HER3双抗ADC)联合奥希替尼用于一线EGFR突变型局部晚期或转移性非小细胞肺癌Ⅲ期临床试验完成首例受试者入组。截至目前,BL-B01D1正在中国和美国进行约30项针对多种肿瘤类型的临床试验,除此次新入组的临床试验外,BL-B01D1在肺癌、乳腺癌、鼻咽癌、食管鳞癌等7项国内III期注册临床试验也处于受试者入组的阶段。
2025-02-18 16:54
【百利天恒:药品获得II/III期临床试验批准通知书)用于HER2阳性乳腺癌新辅助治疗获得II/III期临床试验批准】18日讯,百利天恒公告称,公司于近日收到国家药品监督管理局(NMPA)正式批准签发的《药物临床试验批准通知书》,公司自主研发的创新生物药注射用BL-M07D1(HER2-ADC)的II/III期临床试验获得批准。截至本公告披露日,除本次新获得批准的临床试验外,BL-M07D1正于中国及美国的10项I/II/III期临床试验中作为单药或联用进行评估。各项临床研究包括各种HER2表达/突变的实体瘤(包括非小细胞肺癌、乳腺癌、尿路上皮癌、妇科肿瘤及消化道肿瘤)的患者。
2025-02-18 16:51
百利天恒:注射用BL-M07D1(HER2-ADC)用于HER2阳性乳腺癌新辅助治疗获得II/III期临床试验批准通知书。
2025-02-07 16:38
百利天恒:注射用BL-M07D1(HER2-ADC)用于在新辅助治疗后存在浸润癌残留的HER2阳性乳腺癌术后辅助治疗获得III期临床试验批准通知书。
2025-01-02 16:56
【百利天恒:注射用BL-B01D1被药审中心纳入突破性治疗品种名单】2日讯,百利天恒公告,公司自主研发的创新生物药注射用BL-B01D1已被国家药品监督管理局药品审评中心纳入突破性治疗品种名单。该药拟定适应症为既往经含铂化疗及抗PD-1/PD-L1单抗治疗失败的复发性小细胞肺癌患者。BL-B01D1是全球首创也是唯一进入临床阶段的靶向EGFR×HER3的双抗ADC,目前正在中国和美国进行超过20项针对多种肿瘤类型的临床试验。公司将按有关规定积极推进上述研发项目,并及时履行信息披露义务。
2025-01-02 16:52
百利天恒:注射用BL-B01D1用于既往经含铂化疗及抗PD-1/PD-L1单抗治疗失败的复发性小细胞肺癌患者纳入突破性治疗品种名单。
2024-11-28 17:59
百利天恒:注射用BL-M08D1(ADC)项目治疗复发或难治性血液系统恶性肿瘤和局部晚期或转移性实体瘤获得药物临床试验批准通知书
2024-10-13 16:17
【百利天恒:BL-M11D1临床试验申请获得美国FDA许可】百利天恒公告,近日全资子公司SystImmune,Inc.收到美国食品药品监督管理局(简称“FDA”)的通知,BL-M11D1(CD33-ADC)用于治疗复发或难治性急性髓系白血病患者的I期临床试验申请已获得FDA许可。此次BL-M11D1临床研究获得FDA的IND许可,将进一步推进公司业务和产品国际化布局的进程。
2024-10-09 15:39
百利天恒:公司自主研发的创新生物药注射用BL-B01D1用于既往经PD-1/PD-L1单抗联合含铂化疗治疗失败的复发性或转移性食管鳞癌患者已被国家药品监督管理局药品审评中心纳入突破性治疗品种名单,近日已完成公示。
2024-09-22 15:42
【百利天恒:公司自主研发的多特异性抗体GNC-077临床试验申请获批准】百利天恒公告,公司近日收到国家药品监督管理局(NMPA)正式批准签发的《药物临床试验批准通知书》,公司自主研发的创新生物药多特异性抗体GNC-077的药物临床试验获得批准。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 揭秘股市中的吸筹冲击波:精准捕捉主力建仓信号
- 认清孕十字星,把握股市起涨先机
- 掌握股市风向标:深入解析移动平均数及其运用
- 基本面分析实战指南:四步筛选优质股
- 加仓策略深度剖析:精准把握投资时机与风险控制
- 从三千到百万:黄老太的股市传奇
- 短线炒股的智慧:精准把握六大原则
- 股市操作指南:如何巧妙止损与合理出货
- 散户解套策略全解析
- 股市迷雾:揭秘主力常用的三大骗术
- 股市智慧:解锁不同类型股票的盈利策略
- 揭秘技术分析:战胜“骗线”,精准捕捉买入时机
- 股市智慧:掌握三大止损策略,稳健航行于资本海洋
- 老散户的智慧:揭秘股市成功的十大黄金法则
- 熊市历程:老股民的血泪教训与市场沉浮
- 次新股炒作深度剖析与实战攻略
- 揭秘股市庄股识别术:深度解析十大流通股东名单的奥秘
- 揭秘打板高手的成功之道:精准捕捉“一进二”机遇
- 超短操作的艺术:精准把握“不强不进,不涨就走”的实战策略
- 精准选股策略:五大关键指标解析
当前版本:V3.0

 VIP复盘网
VIP复盘网
