
扫码报名
|
诺诚健华
688428 |
-0.98%
|
最新:12.16
开盘:12.32 昨收:12.28 |
开盘%:0.33%
振幅%:5.29% 换手%:1.69% |
最高:12.65
最低:12 量比:0.96 |
总市值:214 亿
流通值:32 亿 成交额:3 亿 |
- 基本信息
- 个股快讯
- 上市公司
- 龙虎榜
- 历史涨停原因
- 董秘互动
- 分时图
- 日K图
- 周K图
- 月K图
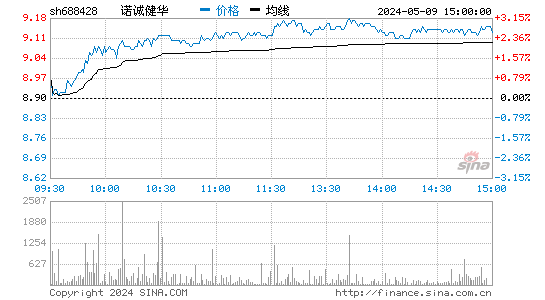
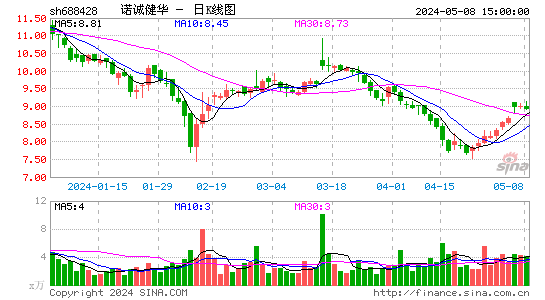
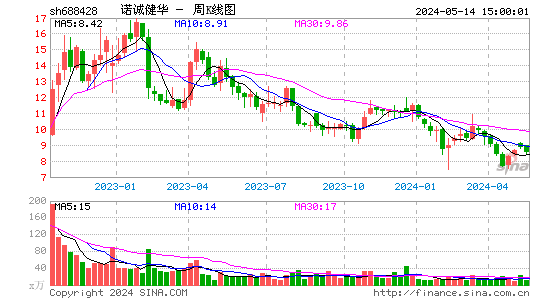
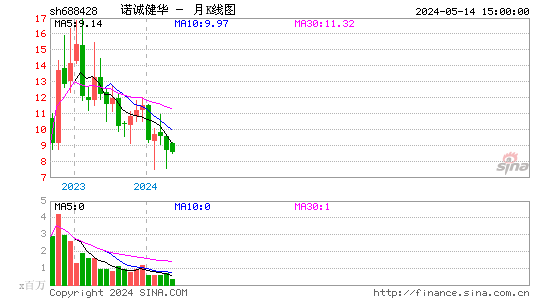
2024-11-11 17:06
【诺诚健华三季报:1-9月净亏损为2.85亿元,比上年同期亏损收窄47.1%】诺诚健华公告,2024 年 1-9 月公司总营业收入 6.98 亿元,比上年同期增长 29.8%。同时,公司持续提高毛利水平,2024 年 1-9 月毛利率为 86.0%,比上年同期的 81.2%提高了 4.8 个百分点。公司 2024 年 1-9 月的净亏损为 2.85 亿元,比上年同期亏损收窄 47.1%。公司核心产品奥布替尼(宜诺凯®)2024年第三季度实现销售收入2.76亿元,同比增长75.5%,2024 年 1-9 月共实现其销售收入 6.93 亿元,同比增长 45.0%。
2024-10-04 16:35
【诺诚健华:奥布替尼治疗系统性红斑狼疮II期临床试验完成患者入组】诺诚健华今日宣布,公司研发的新型BTK抑制剂奥布替尼治疗系统性红斑狼疮(SLE)的II期临床试验完成患者入组。这是一项随机、双盲、安慰剂对照、多中心的IIb期临床研究,旨在评估奥布替尼在成人SLE患者中的有效性和安全性。该研究总共入组187例患者,治疗时间为48周。(证券时报)
2024-09-09 08:18
【诺诚健华与美国FDA成功召开EOP2会议 同意启动奥布替尼治疗原发进展型多发性硬化III期临床研究】9月8日,诺诚健华宣布,公司与美国食品药品监督管理局(FDA)就奥布替尼治疗多发性硬化(MS)的临床开发进展成功召开临床II期结束会议(EOP2),同意启动奥布替尼治疗原发进展型多发性硬化(PPMS)的III期临床研究,FDA同时建议启动奥布替尼治疗继发进展型多发性硬化(SPMS)的III期临床研究,以解决多发性硬化(MS)患者尚未满足的巨大医疗需求。(证券时报)
2024-09-08 17:27
【诺诚健华:与FDA就奥布替尼在PPMS患者中启动三期临床研究达成一致】9月8日电,诺诚健华公告,近日,公司成功完成与美国食品药品监督管理局(简称“FDA”)关于奥布替尼治疗多发性硬化症(简称“MS”)临床开发的“临床2期结束后”会议,并与FDA就奥布替尼在原发进展型多发性硬化症(简称“PPMS”)患者中启动三期临床研究达成一致。这是公司致力于开发创新有效疗法,以满足MS患者未被满足临床需求的一个重要里程碑。FDA还建议公司启动第二项三期临床试验,针对继发进展型多发性硬化症。公司将加速上述项目的进展,致力于将这些急需的疗法尽快带给MS患者以改善他们的生活质量。
2024-08-20 19:51
【诺诚健华:上半年净利润-2.68亿元 亏损缩窄】《科创板日报》20日讯,诺诚健华发布2024年半年度报告,公司上半年实现净利润-2.68亿元,相较去年同期(净利润-4.29亿元)亏损缩窄。公司净利润仍为负,主要由于新药研发、生产、商业化是一个周期长、投资大、风险高的过程,公司在药物早期发现、临床前研究、临床开发、注册、生产、商业化推广等多个环节持续投入。报告期内,公司持续加大在新技术平台建设,临床前研究及临床试验方面的投入,研发投入为4.21亿元,较上年同期增加0.60亿元。
2024-07-24 17:34
【诺诚健华:ICP-332在美国完成首例受试者给药】诺诚健华(688428)7月24日晚间公告,公司创新药ICP-332在美国完成首例受试者给药。ICP-332已在中国完成治疗AD的临床II期研究并取得积极结果。
2024-06-20 19:41
【诺诚健华:公司创新药生物制品许可获受理】6月20日电,诺诚健华公告,公司创新药tafasitamab(坦昔妥单抗)与来那度胺联合治疗不适合作自体干细胞移植(ASCT)的复发或难治性弥漫性大B细胞淋巴瘤(DLBCL)的成年患者的生物制品许可(BLA),近日已获国家药品监督管理局(NMPA)药品审评中心(CDE)受理并纳入优先审评。
2024-05-31 18:12
【诺诚健华:行政总裁崔霁松增持公司31.6万股股份】5月31日电,诺诚健华公告,公司行政总裁兼执行董事崔霁松增持公司股份。崔霁松告知公司,彼于5月30日动用个人资金在公开市场购买合共31.6万股股份。增持股份后,崔霁松及其家族于公司合共持有的股权占截至公告日期公司已发行股份总数约7.16%。
2024-05-13 19:10
【诺诚健华:2024年一季度净利润亏损1.42亿元】诺诚健华5月13日发布一季度报告,2024年一季度实现营业收入1.66亿元,同比下降12.44%;净利润亏损1.42亿元。净利润下降主要原因如下:汇率变动导致未实现汇兑由上年的收益转为本年的亏损;研发投入持续增加;研发服务收入较上年同期减少;可转换贷款公允价值亏损较上年同期增加。
2024-03-28 21:56
【诺诚健华2023年收入7.4亿元 毛利上涨26.6%】3月28日,诺诚健华发布了截至2023年12月31日的2023年业绩报告。报告显示,该公司2023年度收入同比增长了18.1%,达到了7.4亿元;毛利同比增长了26.6%,达到了6.1亿元。同时,公司2023年亏损同比缩小了27.8%,降至6.5亿元,而截至2023年12月31日的现金和银行结余达到了82.2亿元。
2024-03-13 13:50
【诺诚健华:BCL2抑制剂ICP-248联合奥布替尼一线治疗CLL/SLL获批临床】诺诚健华官微3月13日宣布,公司自主研发的BCL2抑制剂ICP-248联合布鲁顿酪氨酸激酶(BTK)抑制剂奥布替尼一线治治慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)在中国获批临床。
2024-03-11 09:19
【诺诚健华:ICP-332治疗特应性皮炎最新数据在2024年美国皮肤病学会年会以重磅口头报告发布】诺诚健华3月11日宣布,公司自主研发的新型TYK2抑制剂ICP-332治疗中重度特应性皮炎(AD)II期临床的最新数据在2024年美国皮肤病学会年会(2024 AAD Annual Meeting)以重磅口头报告(late-breaking oral presentation)形式发布。(证券时报)
2024-01-24 20:05
【诺诚健华:创新药ICP-723近日完成首例儿童患者给药】诺诚健华(688428)1月24日晚间发布了关于创新药zurletrectinib(ICP-723)临床试验进展的公告。目前,zurletrectinib(ICP-723)已进入注册性临床阶段。该药物在成人和青少年患者(12周岁到18周岁)中展示出良好的安全性和有效性。最近,该药物还完成了首例儿童患者(2周岁到12周岁)的给药,这是首次在儿童患者中启动临床研究。
2023-12-17 15:34
【诺诚健华:ICP-332 Ⅱ期临床试验取得了积极的临床试验结果】12月17日电,诺诚健华公告,公司创新药ICP-332在中重度特应性皮炎成年患者中进行的Ⅱ期随机、双盲、安慰剂对照研究中取得了积极的临床试验结果。
2023-12-01 13:39
【诺诚健华:获纳入MSCI中国全股票小盘指数 11月30日收盘后生效】12月1日电,诺诚健华今日宣布,公司被纳入国际知名指数公司MSCI(Morgan Stanley Capital International) 中国全股票小盘指数(MSCI China All Shares Small Cap Index),这一结果已于2023年11月30日收盘后生效。
2023-09-14 11:15
【诺诚健华:SHP2抑制剂ICP-189联用EGFR抑制剂伏美替尼获批临床】诺诚健华今日宣布,新型蛋白酪氨酸磷酸酶SHP2变构抑制剂ICP-189联用针对表皮生长因子受体(EGFR)突变的口服EGFR激酶抑制剂伏美替尼在中国获批开展临床试验。(证券时报)
2023-06-20 14:15
【港股生物技术股集体下跌 药明生物跌超14%】6月20日电,港股生物科技股集体下跌。截至发稿,药明生物(02269.HK)跌14%,诺诚健华(09969.HK)跌超7%,金斯瑞生物科技(01548.HK)跌超6%。
2023-04-11 09:38
【港股生物医药股多数上涨 荣昌生物涨超8%】4月11日电,截至发稿,荣昌生物-B(09995.HK)涨8.51%、加科思-B(01167.HK)涨8.05%、诺诚健华-B(09969.HK)涨7.42%、康诺亚-B(02162.HK)涨7.24%。
2023-04-04 09:04
【诺诚健华:新型分子胶靶向蛋白降解剂ICP-490完成首例受试者给药】诺诚健华今日宣布,公司自主研发的新型分子胶靶向蛋白降解剂ICP-490在中国完成首例受试者给药。ICP-490是诺诚健华自主研发的创新药,源自公司的分子胶平台,旨在治疗多发性骨髓瘤(MM)、非霍奇金淋巴瘤(NHL)等血液肿瘤。与前几代免疫调节剂相比,ICP-490活性显著增强,可以克服前几代免疫调节剂的耐药性,能够通过调节免疫增强多种单抗药物疗效,为临床联用提供了强有力的理论支持,在血液肿瘤领域展现了强劲的潜力。
2023-02-16 16:44
【龙虎榜|诺诚健华今日跌18.37% 五机构净卖出2.43亿元】2月16日电,诺诚健华今日跌18.37%,成交额6.03亿元,换手率20.74%,盘后龙虎榜数据显示,五机构净卖出2.43亿元。
2023-02-16 09:25
【诺诚健华港股低开近15%】诺诚健华港股低开近15%,渤健退回诺诚健华BTK抑制剂全球权益。
2023-02-15 17:49
诺诚健华:公司重获奥布替尼全球权利
2022-12-23 20:42
【诺诚健华:暂停评估奥布替尼治疗多发性硬化症的Ⅱ期临床研究患者招募】《科创板日报》23日讯,诺诚健华公告,美国食品药品监督管理局(FDA)已对公司奥布替尼用于治疗多发性硬化症(MS)的Ⅱ期临床研究实施部分临床搁置。因此,在美国进行的该临床研究不会开展新的患者招募。FDA此次行动是基于在使用奥布替尼的进行中的多发性硬化症(MS)Ⅱ期临床研究及其他非多发性硬化症(MS)自身免疫性疾病的研究中,观察到有限数目的药物导致肝损伤的病例。所有病例在停用奥布替尼后,监测肝损伤的实验室数值升高均可逆转。公司将与FDA紧密合作以解决这项问题,包括实施更完善的安全措施。

 VIP复盘网
VIP复盘网
