
扫码关注公众号
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
海创药业
688302 |
3.33%
|
最新:42.2
开盘:40.84 昨收:40.84 |
开盘%:0%
振幅%:7.52% 换手%:9.96% |
最高:43.4
最低:40.33 量比:1.98 |
总市值:42 亿
流通值:31 亿 成交额:1 亿 |
- 基本信息
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- Deepseek分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
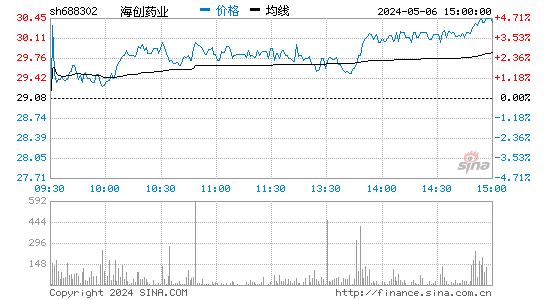
- 分时图
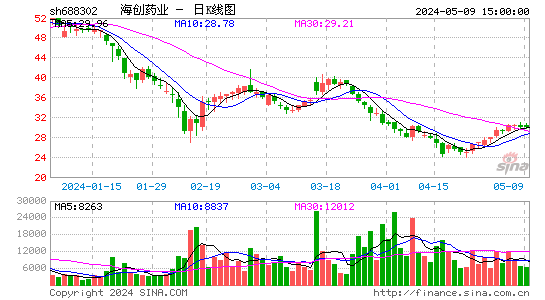
- 日K图
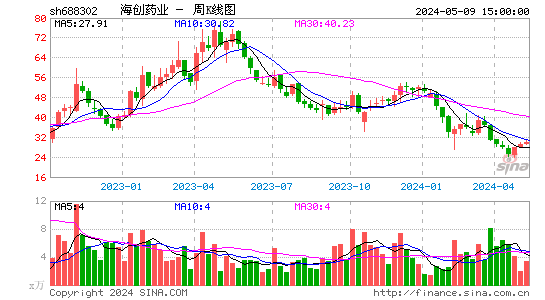
- 周K图
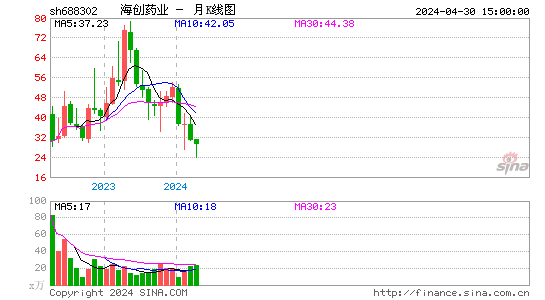
- 月K图
海创药业-U股票详解
探索创新药物企业的股市表现与前景
公司概况
海创药业-U,全称为海创药业股份有限公司,是一家专注于癌症和代谢性疾病药物研发的创新型企业。公司成立于2013年,总部位于四川成都,并于2022年在科创板成功上市。其股票代码为688302,因上市时尚未盈利,证券简称带“U”。
研发实力
创新平台:海创药业拥有PROTAC靶向蛋白降解技术平台、氘代药物研发平台等多个创新平台,致力于开发具有重大临床需求的Best-in-class和First-in-class药物。
在研管线:公司在研管线丰富,包括HP515、HP568等多个针对代谢性疾病和癌症的创新药物。其中,HP515已在美国获得FDA批准,用于治疗代谢性脂肪性肝炎。
市场表现
海创药业-U自上市以来,股价波动较大。近年来,随着公司在研药物的临床进展和市场对其创新能力的认可,股价逐渐企稳。然而,由于尚未实现盈利,公司仍面临较大的市场压力和退市风险。
未来展望
海创药业将继续加大研发投入,推动在研药物的临床进展和上市申请。同时,公司也将积极寻求合作伙伴,拓展国内外市场,以实现可持续发展。
总结:海创药业-U作为一家专注于创新药研发的企业,拥有强大的研发实力和丰富的在研管线。虽然目前尚未盈利,但随着在研药物的逐步推进和市场对其创新能力的认可,公司未来发展前景值得期待。
2025-01-19 15:45
【海创药业:HP515片中国临床试验完成首例受试者入组】海创药业公告,公司自主研发的HP515片用于治疗非酒精性脂肪性肝炎(NASH)的临床试验于近日完成首例受试者入组。
2025-01-09 18:43
【海创药业:自主研发的HP568片中国临床试验完成首例受试者入组】1月9日电,海创药业公告,公司自主研发的HP568片用于治疗ER+/HER2-晚期乳腺癌的临床试验于近日完成首例受试者入组。HP568片是公司自主研发的口服雌激素受体α蛋白降解靶向联合体药物,该适应症的临床试验申请于2024年10月获得中国国家药品监督管理局批准,并于2024年12月获得美国食品药品监督管理局批准。该研究是一项评估口服HP568片单药和联合哌柏西利在ER+/HER2-晚期乳腺癌患者中的安全性、耐受性、药代动力学和初步疗效的多中心、开放、剂量递增/剂量拓展、Ⅰ/Ⅱ期临床研究。公司将积极推进上述研发项目,并严格按照有关规定及时对项目后续进展情况履行信息披露义务。
2024-12-30 15:38
海创药业:口服PROTAC药物HP568片用于治疗ER+/HER2-晚期乳腺癌的临床试验申请获得美国FDA批准
2024-12-04 21:22
【海创药业:股东盈创动力拟减持不超过3%公司股份】海创药业公告称,公司持股5%以上的股东成都盈创动力创业投资有限公司(简称“盈创动力”)计划自本公告披露之日起十五个交易日后的三个月内,通过集中竞价交易方式和大宗交易方式减持公司股份合计不超过297.05万股,减持比例不超过公司总股本的3%。
2024-10-15 17:47
【海创药业:HP568片获临床试验批准】海创药业公告,公司收到国家药品监督管理局药品审评中心核准签发的《药物临床试验批准通知书》,同意HP568片开展用于治疗雌激素受体阳性和人表皮生长因子受体2阴性的晚期乳腺癌的临床试验。HP568是公司自主研发的靶向降解雌激素受体α的口服蛋白降解靶向联合体药物,由靶蛋白配体、E3连接酶配体和两配体间的连接子3部分构成,拟用于治疗ER+/HER2-晚期乳腺癌。
2024-09-13 17:05
【海创药业:HP515片用于治疗代谢性脂肪性肝炎的临床试验申请获FDA批准】9月13日电,海创药业公告,公司收到美国FDA的临床研究继续进行通知书,公司自主研发的HP515片用于治疗代谢性脂肪性肝炎(MASH)的临床试验申请正式获得FDA批准。HP515是公司自主研发的一种口服高选择性THR-β激动剂,拟用于治疗代谢性脂肪性肝炎(MASH)。
2024-08-27 22:40
【海创药业:HP515片用于治疗非酒精性脂肪性肝炎的临床试验获批】海创药业8月27日晚间公告,近日公司收到国家药监局药品审评中心核准签发的《药物临床试验批准通知书》,同意HP515片开展用于治疗非酒精性脂肪性肝炎的临床试验。经查询,截至目前,国内无同类靶点产品获批上市。
2024-08-27 17:26
【海创药业:HP515片用于治疗非酒精性脂肪性肝炎的临床试验获得批准】《科创板日报》27日讯,海创药业公告,公司收到中国国家药品监督管理局药品审评中心核准签发的《药物临床试验批准通知书》,同意HP515片开展用于治疗非酒精性脂肪性肝炎的临床试验。HP515是公司自主研发的一种口服高选择性THR-β激动剂,能直接作用于THR-β激活下游基因转录,通过增强肝细胞脂质代谢活性、提高肝脏脂肪代谢、降低脂毒性达到对非酒精性脂肪性肝炎的改善效果。截至公告披露日,国内尚无同类靶点产品获批上市。
2024-07-24 17:39
【海创药业:HP560片用于治疗骨髓纤维化(骨髓增殖性肿瘤)的临床试验获批】海创药业(688302)于7月24日晚间宣布,一项重要的里程碑取得进展:公司获得国家药品监督管理局药品审评中心批准签发的《药物临床试验批准通知书》,标志着HP560片用于治疗骨髓纤维化的临床试验正式获准启动。
2024-07-07 16:48
【海创药业:HP537片用于治疗血液系统恶性肿瘤的临床I/II期试验申请获得美国FDA批准】7月7日电,海创药业公告,公司自主研发的HP537片用于治疗血液系统恶性肿瘤的临床I/II期试验申请正式获得FDA批准。此前,HP537片中国临床试验申请已于2024年2月获国家药品监督管理局批准。经查询,截至本公告披露日,国内外均无同类靶点产品获批上市。
2024-06-30 16:25
【海创药业:HP518片拟用于治疗雄激素受体(AR)阳性三阴乳腺癌获美国FDA授予快速通道认定】海创药业6月30日晚间公告,近日公司在研品种HP518片收到美国食品药品监督管理局(简称“FDA”)授予“快速通道认定”用于治疗雄激素受体(AR)阳性三阴乳腺癌。目前国内外均无同类靶点产品获批上市。
2024-06-21 21:17
【海创药业:盈创动力拟减持不超1%股份】6月21日电,海创药业公告,持股9.6552%的股东盈创动力计划自公告披露之日起15个交易日后的三个月内,通过集中竞价方式合计减持公司股份不超过99.015万股,即不超过公司总股本的1%。
2024-05-27 16:49
【海创药业:PROTAC在研药物HP518在2024年美国临床肿瘤学会年会发布临床数据】5月27日电,海创药业公告,公司自主研发的PROTAC在研创新药物HP518的临床研究数据将在2024年美国临床肿瘤学会(ASCO)年会上发布。该药物用于晚期前列腺癌(mCRPC)患者治疗。
2024-05-27 16:44
海创药业:PROTAC在研药物HP518在2024年美国临床肿瘤学会年会发布临床数据,HP518在mCRPC患者中显示出积极的疗效,支持开展下一步临床研究。
2024-04-26 15:52
【海创药业:一季度净利润亏损4721.48万元】4月26日电,海创药业披露一季报,2024年第一季度营业收入0元,净利润亏损4721.48万元。
2024-02-22 18:23
海创药业:治疗血液系统恶性肿瘤的HP537片获得药物临床试验批准通知书
2023-12-27 16:39
海创药业:口服PROTAC药物HP518片中国临床试验完成首例受试者入组。
2023-12-10 16:19
【海创药业:HP537获得临床试验申请受理通知书】12月10日电,海创药业公告,近日,公司收到国家药品监督管理局核准签发的《受理通知书》,公司自主研发的HP537片用于治疗血液系统恶性肿瘤,包括但不限于多发性骨髓瘤、非霍奇金淋巴瘤、急性髓系白血病、骨髓增生异常综合征的临床试验申请获得受理。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- MACD指标深度解析与应用策略
- 活用EXPMA指标:精准捕捉股市机遇
- 股市解套策略:三大战法深度剖析与实战应用
- 股市智慧:掌握七大原则,精准布局股票投资
- 尾盘选股的艺术:掌握高开个股的秘诀
- 投资之道:不止损的智慧与策略
- 低位补仓的艺术:策略、技法与陷阱识别
- 揭秘K线力学:七大技巧助你捕获短线黑马
- 揭秘股市中的大抛单:策略、动机与市场影响
- 股市新手困惑:如何避免一买就跌,一卖就涨?
- A—H溢价率的市场意义深度剖析
- MACD指标的深度解析与应用策略
- 股市江湖:揭秘炒股四大门派与财富之道
- 股市高手的炒股智慧:口诀引领投资之道
- 新股淘金:深度解析大户炒新策略与市场变迁
- 揭秘股市“芝麻开花”K线形态与逼空式拉升策略
- 《主线龙头战法》及其底层逻辑深度剖析
- 波段操作的艺术:五大黄金原则引领股市航行
- 揭秘庄家八大洗盘骗术:投资者必看的防骗指南
- 揭秘券商内部行情判断秘籍:多维度解析市场趋势
当前版本:V3.0

 VIP复盘网
VIP复盘网
