
扫码关注公众号

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
泽璟制药
688266 |
0.33%
|
最新:114.92
开盘:116.29 昨收:114.54 |
开盘%:1.53%
振幅%:4.37% 换手%:1.17% |
最高:116.5
最低:111.5 量比:0.64 |
总市值:304 亿
流通值:304 亿 成交额:3 亿 |
- 基本信息
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
- 分时图
- 日K图
- 周K图
- 月K图
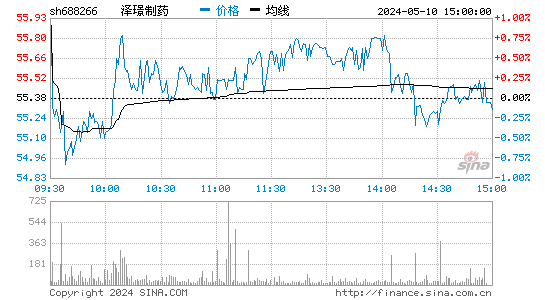
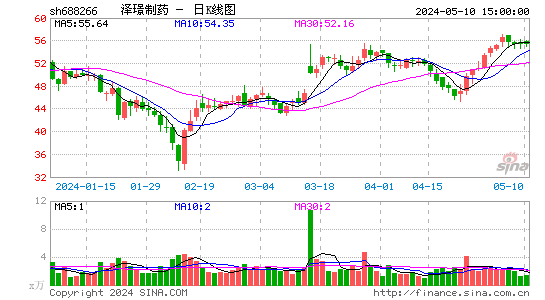
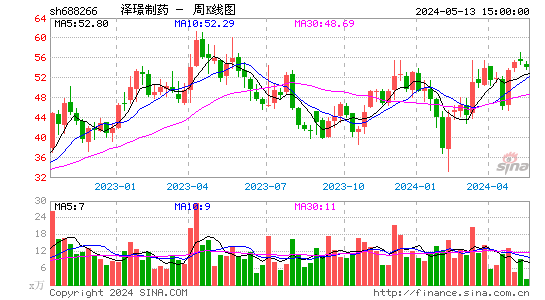
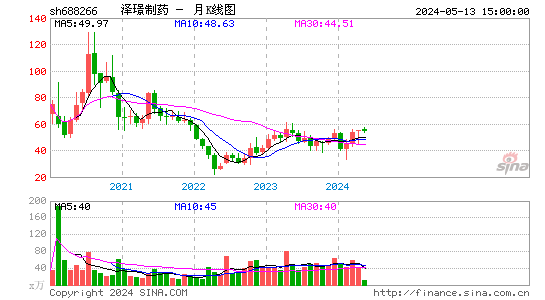
泽璟制药-U股票概况
探索创新药物研发领域的领军企业
一、公司概况
泽璟制药-U,股票代码688266,全称苏州泽璟生物制药股份有限公司,成立于2009年3月18日,并于2020年1月23日在科创板上市。公司总部位于江苏省昆山市,法定代表人为ZELIN SHENG(盛泽林)。
二、研发管线
泽璟制药-U的核心业务是创新药物的自主研发。公司的研发管线涵盖了肿瘤、出血及血液疾病、免疫炎症性疾病和肝胆疾病等多个治疗领域。
三、市场表现
泽璟制药-U的股价在近年来呈现出波动上涨的趋势。虽然公司目前尚未实现盈利,但其在创新药物研发领域的投入和成果逐渐得到市场的认可。
四、未来展望
展望未来,泽璟制药-U将继续深耕创新药物研发领域,扩大研发管线,加强国际合作,推动更多新药上市,为全球患者提供更多优质的治疗选择。
总结:
泽璟制药-U作为科创板上的创新药物研发企业,凭借其丰富的研发管线和明确的战略规划,在肿瘤、出血及血液疾病等领域展现出巨大的发展潜力。未来,公司有望成为全球创新药物研发领域的佼佼者。
2025-05-29 15:54
【泽璟制药:盐酸吉卡昔替尼片获批上市】29日讯,泽璟制药(688266.SH)公告称,公司自主研发的盐酸吉卡昔替尼片(商品名:泽普平)的新药上市申请获得批准,适应症为“用于中危或高危原发性骨髓纤维化(PMF)、真性红细胞增多症继发性骨髓纤维化(PPV-MF)和原发性血小板增多症继发性骨纤维化(PET-MF)的成人患者,治疗疾病相关脾肿大或疾病相关症状”。这是盐酸吉卡昔替尼片首个获批的临床适应症,也是首个获批用于治疗骨髓纤维化的国产JAK抑制剂类创新药物。盐酸吉卡昔替尼片的获批上市预计将对公司未来经营业绩产生积极影响,但具体销售情况受多种因素影响,存在不确定性。
2025-05-13 16:21
泽璟制药:盐酸吉卡昔替尼片治疗重度斑秃的新药上市申请获得受理
2025-05-13 16:20
【泽璟制药:盐酸吉卡昔替尼片治疗重度斑秃的新药上市申请获得受理】13日讯,泽璟制药(688266.SH)公告称,公司收到国家药品监督管理局核准签发的《受理通知书》,公司递交的盐酸吉卡昔替尼片治疗重度斑秃的新药上市申请(NDA)获得受理。这是盐酸吉卡昔替尼片第二个申请新药上市的适应症。盐酸吉卡昔替尼是一种新型的JAK抑制剂,对JAK激酶的四个亚型JAK1、JAK2、JAK3和TYK2都有显著的抑制作用。本次获得NDA受理的适应症是用于治疗重度斑秃,是盐酸吉卡昔替尼片第二个申请新药上市的适应症。在我国,目前尚无国产JAK抑制剂类药物获批用于治疗重度斑秃。
2025-04-20 15:39
泽璟制药:注射用ZG006与PD-1/PD-L1免疫检查点抑制剂联用获得药物临床试验批准通知书
2025-04-09 15:54
泽璟制药:注射用ZG005与化疗联用获得药物临床试验批准通知书
2025-02-17 17:50
【泽璟制药:注射用ZG005与含铂化疗方案联用获得药物临床试验批准通知书】《科创板日报》17日讯,泽璟制药公告称,公司收到国家药监局核准签发的《药物临床试验批准通知书》,注射用ZG005与含铂化疗方案联合用于晚期胆道癌患者的临床试验获得批准。本次临床试验获批事项对公司近期业绩不会产生重大影响。由于药品研发周期长、审批环节多、研发投入大,存在无法获批上市销售的风险,敬请广大投资者谨慎决策,注意防范投资风险。
2025-02-17 17:48
泽璟制药:注射用ZG005与含铂化疗方案联用获得药物临床试验批准通知书
2024-12-25 16:29
泽璟制药:注射用ZG005与盐酸吉卡昔替尼片联合用药获得药物临床试验批准通知书
2024-11-28 16:44
泽璟制药:重组人凝血酶纳入2024年国家医保药品目录
2024-08-12 15:41
泽璟制药:根据《药品注册管理办法》有关规定,国家药品监督管理局食品药品审核查验中心(CFDI)将对公司申报注册的注射用重组人促甲状腺激素启动药品注册核查(药学、临床),后续待通过现场核查、抽样检验、综合审评审批后才能取得上市注册批件
2024-08-08 15:38
泽璟制药:公司在研产品注射用ZG006获得美国食品药品监督管理局颁发孤儿药资格认定(Orphan-drug Designation),用于治疗小细胞肺癌。
2024-08-05 16:26
泽璟制药:近日收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,注射用ZG005与贝伐珠单抗联合用于晚期肝细胞癌的临床试验获得批准。
2024-08-05 16:06
【泽璟制药:注射用ZG005与ZGGS18联合用药获临床试验批准】《科创板日报》5日讯,泽璟制药公告,公司近日收到国家药监局核准签发的《药物临床试验批准通知书》,注射用ZG005与注射用ZGGS18联合用于晚期实体瘤的临床试验获得批准。同日公告,注射用ZG005与贝伐珠单抗联合用于晚期肝细胞癌的临床试验获得批准。
2024-08-01 20:08
【泽璟制药:盐酸吉卡昔替尼片治疗特发性纤维化II期临床试验取得成功结果】泽璟制药(688266)8月1日晚间公告,近日,公司自主研发的1类新药盐酸吉卡昔替尼片(曾用名:盐酸杰克替尼片)治疗特发性纤维化的II期临床研究取得成功结果。结果显示,24周时吉卡昔替尼片两个剂量组(50mg Bid和75mg Bid)相较安慰剂组均可大幅度延缓受试者用力肺活量(FVC)的下降。各剂量组的耐受性和安全性良好。该试验是全球首个JAK抑制剂在特发性纤维化患者中完成的II期临床研究。
2024-06-12 16:39
【泽璟制药:盐酸吉卡昔替尼片治疗重症斑秃Ⅲ期临床试验达到主要疗效终点】泽璟制药公告,近日公司自主研发的1类新药盐酸吉卡昔替尼片(曾用名:盐酸杰克替尼片)治疗重症斑秃的Ⅲ期临床主试验《盐酸杰克替尼片治疗重症斑秃患者的有效性和安全性的多中心、随机、双盲、安慰剂平行对照III期临床试验》达到了主要疗效终点,达到统计显著性(p<0.0001)。公司将加快推进盐酸吉卡昔替尼片治疗重症斑秃患者适应症的上市进程。
2024-06-03 16:03
泽璟制药:递交注射用重组人促甲状腺激素生物制品上市许可申请。
2024-05-29 16:03
泽璟制药:盐酸吉卡昔替尼片获得药物临床试验批准通知书
2024-04-11 15:37
泽璟制药:盐酸杰克替尼乳膏获得药物临床试验批准通知书
2024-01-02 16:31
泽璟制药:重组人凝血酶获批上市。
2023-12-13 17:16
泽璟制药:甲苯磺酸多纳非尼片续约并新增适应症纳入国家医保目录。
2023-11-20 15:07
【泽璟制药:公司目前正在开展ZG005的后续扩展临床研究】泽璟制药近期在接受调研时表示,公司已经完成ZG005的I期剂量爬坡研究,临床结果显示ZG005具备良好的安全性。在今年的ASCO会议上,公司披露了ZG005的Ia期临床的部分结果,在可评估的时间段内,展现了良好的抗肿瘤效果,对于已经抗PD-1或抗PD-L1等肿瘤免疫药物或多线抗肿瘤药物治疗的患者,DCR达到60%以上,在特定肿瘤中也看到了客观响应。公司目前正在开展ZG005的后续扩展临床研究。
2023-11-03 16:10
【泽璟制药:公司副总经理辞职】泽璟制药公告,董事会于近日收到公司副总经理 JUNLI ZHANG(张均利)的书面辞职报告,JUNLI ZHANG(张均利)因个人原因申请辞去公司副总经理职务,其辞职报告自送达公司董事会之日起生效。辞职后,JUNLI ZHANG(张均利)将不再担任公司任何职务,其辞任副总经理职务不会影响公司的正常工作及生产经营。
2023-09-21 17:07
【泽璟制药:ZG005粉针剂与甲苯磺酸多纳非尼片联用获得药物临床试验批准通知书】《科创板日报》21日讯,泽璟制药公告,收到国家药监局核准签发的《药物临床试验批准通知书》,ZG005粉针剂与甲苯磺酸多纳非尼片(商品名:泽普生®)联合用于实体肿瘤的临床试验获得批准。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 股市风险与机遇并存:老股民给辞职炒股者的十大忠告
- MACD指标深度解析:掌握股市脉动的关键工具
- 专业化投资:解锁盈利的五大关键策略
- 操盘手绝密利器全解析
- 基本面选股:稳健投资者的炒股策略
- 如何成为股市中的顶尖龙头猎手
- 止损策略的十二要决与实操分析
- 选股智慧:动态把握热点,技术分析的实战运用
- 超级散户的智慧:高手与低手的投资策略解析
- 利率变动下的期权价值波动:深度剖析与策略应对
- 股市风云:揭秘领涨板块的形成与实战策略
- KDJ指标实战解析:精准捕捉买卖点
- 揭秘股市“阳阴墓碑”形态:精准识别庄家出货信号
- 股市趋势线分析:探寻牛市踪迹
- 资深股民揭秘:精准捕捉强势股的实战策略
- 交易市场的心灵博弈:从赌徒心态到理性投资的觉醒
- 掌握选股策略,投资未来赢家
- 掌握抄底艺术:深度解析老股民珍藏的九条抄底神技
- 揭秘股市分析利器:DDE指标深度解读
- 揭秘涨停回马枪战法:精准低吸的实战艺术与逻辑剖析
当前版本:V3.0

 VIP复盘网
VIP复盘网
