
扫码关注公众号

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
前沿生物
688221 |
8.26%
|
最新:12.84
开盘:11.91 昨收:11.86 |
开盘%:0.42%
振幅%:12.48% 换手%:7.81% |
最高:13.27
最低:11.79 量比:1.85 |
总市值:48 亿
流通值:48 亿 成交额:4 亿 |
- 基本信息
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
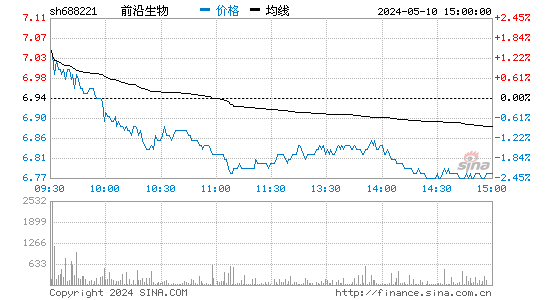
- 分时图
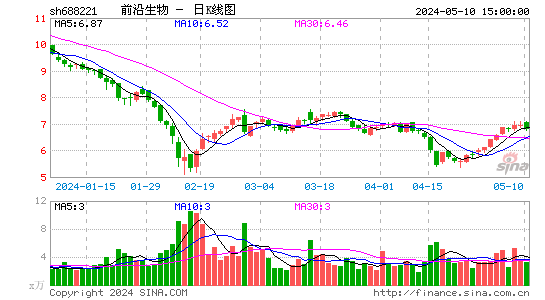
- 日K图
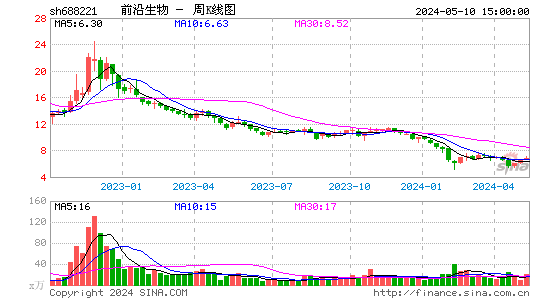
- 周K图
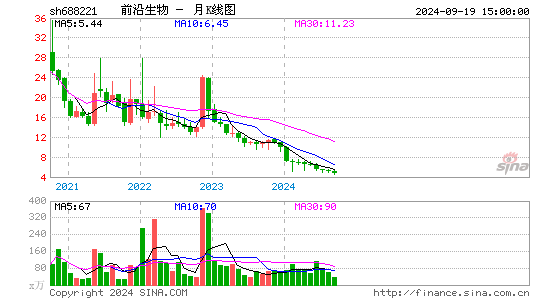
- 月K图
前沿生物-U股票概览
全面解析前沿生物-U的投资价值与前景
公司概况
前沿生物-U是一家专注于生物制药领域的上市公司,致力于研发创新药物,以改善人类健康。公司自成立以来,凭借强大的研发团队和先进的技术平台,在生物制药领域取得了显著成果。
业务领域
创新药物研发:前沿生物-U专注于传染病、肿瘤等重大疾病领域的创新药物研发。公司研发的多个药物已进入临床试验阶段,部分药物已取得突破性进展。
合作与授权:公司与国内外多家知名药企和研究机构建立了合作关系,共同推动创新药物的研发和市场推广。
财务分析
前沿生物-U近年来在研发投入上持续增加,虽然短期内影响了公司的盈利能力,但为公司的长期发展奠定了坚实基础。同时,公司积极拓展融资渠道,降低财务风险。
市场前景
随着全球生物制药市场的持续增长,前沿生物-U有望凭借其在创新药物研发领域的优势,实现业务的快速增长。此外,公司积极拓展国际市场,提升品牌影响力。
总结:
前沿生物-U作为生物制药领域的佼佼者,凭借其在创新药物研发领域的深厚积累,展现了广阔的市场前景。投资者应关注公司的研发进展和市场拓展情况,把握投资机会。
总结:
前沿生物-U作为生物制药行业的佼佼者,拥有强大的研发团队和先进的技术平台,专注于传染病、肿瘤等领域的创新药物研发。公司积极拓展国际市场,降低财务风险,展现了广阔的市场前景。
2025-07-04 15:50
【四川出台方案发展壮大新兴产业 重点突破人工智能、机器人等23个方向】7月4日电,7月4日,四川经信厅官微消息,近日,省政府办公厅印发《关于发展壮大新兴产业加快培育未来产业的实施方案(2025—2027年)》(以下简称《方案》),明确了四川发展新兴产业、培育未来产业的总体目标、重点突破方向和重点任务。《方案》明确了23个重点突破方向,其中15个新兴产业领域,包括人工智能、机器人、集成电路、新型显示、生物医药、核医疗、商业航天、新型航空、低空经济、氢能、新型储能、激光装备、增材制造、生物农业、先进材料等;8个未来产业领域,包括第六代移动通信(6G)、量子科技、元宇宙、前沿生物、脑科学与脑机接口、可控核聚变、超高速轨道交通、深地科学等。
2025-07-04 10:37
【四川出台方案发展壮大新兴产业 加快培育未来产业】7月4日电,四川省政府办公厅近日印发《关于发展壮大新兴产业加快培育未来产业的实施方案(2025—2027年)》,明确了四川发展新兴产业、培育未来产业的总体目标、重点突破方向和重点任务。《方案》提出到2027年,全省新兴产业成链集群发展,培育30家以上具有全国影响力的行业领军企业,打造5个千亿级产业集群、10个五百亿级产业集群;未来产业创新突破发展,培育10家以上高成长创新型企业,涌现一批重大创新成果和标志性产品,产业化能力初步形成。《方案》明确了23个重点突破方向,其中15个新兴产业领域,包括人工智能、机器人、集成电路、新型显示、生物医药、核医疗、商业航天、新型航空、低空经济、氢能、新型储能、激光装备、增材制造、生物农业、先进材料等;8个未来产业领域,包括第六代移动通信(6G)、量子科技、元宇宙、前沿生物、脑科学与脑机接口、可控核聚变、超高速轨道交通、深地科学等。
2025-06-19 17:32
【32家科创板未盈利公司将纳入科创成长层】6月19日电,6月18日,中国证监会发布《关于在科创板设置科创成长层增强制度包容性适应性的意见》,明确设置科创板科创成长层。上海证券交易所起草了《上海证券交易所科创板上市公司自律监管指引第5号——科创成长层(征求意见稿)》(下称《科创成长层指引》),从科创成长层的层次定位、纳入调出条件、信息披露要求、风险揭示等方面作出具体要求。据记者统计,科创板累计已有54家未盈利企业上市。目前已有22家企业上市后实现盈利,还有32家尚未实现摘“U”。根据《科创成长层指引》要求,上述32家公司将自指引(正式稿)发布之日起纳入科创成长层。具体来看,32家尚未摘“U”的存量公司包括:泽璟制药、君实生物、前沿生物、青云科技、和辉光电、精进电动、百济神州、迪哲医药、迈威生物、翱捷科技、亚虹医药、首药控股、海创药业、云从科技、益方生物、奥比中光、盟科药业、诺诚健华、信科移动、星环科技、裕太微、云天励飞、天智航、奇安信、寒武纪、亿华通、埃夫特、慧智微、芯联集成、智翔金泰、盛科通信、中巨芯。(上海证券报)
2025-04-14 09:51
创新药概念反复活跃 ,一品红涨超10%,股价续创历史新高,东诚药业涨停,悦康药业、科兴制药、智翔金泰、前沿生物、热景生物、百济神州等涨幅靠前
2025-04-14 09:51
【创新药概念反复活跃 一品红涨超10%续创历史新高】4月14日电,一品红涨超10%,股价续创历史新高,东诚药业涨停,悦康药业、科兴制药、智翔金泰、前沿生物、热景生物、百济神州等涨幅靠前。消息面上,兴业证券认为,近期,创新药领域催化剂不断,包括海外授权、国内政策和临床数据进展等。预计和去年相比今年国产创新药重要数据将较多,有望为创新药板块带来正面催化。
2025-01-17 16:54
前沿生物:艾可宁新增免疫重建不全适应症获得Ⅱ期临床试验批准通知书
2024-11-28 18:00
【前沿生物:艾可宁续约进入国家医保目录】11月28日电,前沿生物公告,公司独家专利产品艾可宁 续谈成功,纳入《国家基本医疗保险、工伤保险和生育保险药品目录》。艾可宁为全球首个获批的长效HIV融合抑制剂,每周给药一次,具有用药频率低、起效快、耐药屏障高、安全性高、副作用小等特点。医保支付标准维持原支付标准,532元,限定支付范围维持原限定支付范围,限艾滋病病毒感染。本次医保续约将有利于艾可宁 的临床处方,有助于产品在地市和县级市场的下沉和后续产品的销售和商业化推广。
2024-11-06 18:50
【前沿生物:艾可宁®新增原料药供应商 子公司四川前沿通过药品GMP符合性检查】6日讯,前沿生物公告,公司收到国家药品监督管理局核准签发的《药品补充申请批准通知书》,批准艾可宁®新增“四川前沿生物药业有限公司”为原料药供应商。公司子公司四川前沿收到国家药品监督管理局核准签发的《化学原料药上市申请批准通知书》,批准境内生产艾可宁®化学原料药的上市申请。同时,四川前沿收到四川省药品监督管理局签发的《药品GMP符合性检查告知书》,艾可宁®原料药生产线通过药品GMP符合性检查。公司已与四川前沿就艾可宁®原料药的采购签署《艾博韦泰(原料药)采购协议》。
2024-10-10 19:57
【多瑞医药:公司及控股子公司签署股权转让协议】多瑞医药公告,为加快完成原料药产业的延伸布局,为公司寻找新的营收增长点,2024年8月26日,公司与前沿生物、上海建瓴(“标的公司”)签署了《投资意向协议》,公司拟通过股权受让的方式投资标的公司,目标持股比例70%。截至本公告披露日,公司已支付投资意向金1,000.00万元。本次交易完成后,上海建瓴纳入公司的合并报表范围。
2024-10-10 18:25
【前沿生物:拟转让全资子公司上海建瓴70%股权】10日讯,前沿生物公告,为聚焦主业发展、优化资源配置,公司拟将全资子公司上海前沿建瓴生物科技有限公司70%股权转让给昌都市瑞乐康企业管理有限公司,股权转让款为7700.00万元。
2024-09-19 13:03
新冠药概念股午后异动,海创药业、广生堂涨超15%,博瑞医药、前沿生物、新华制药、雅本化学等涨幅居前。
2024-08-27 17:19
【前沿生物:拟将上海建瓴70%股权转让给多瑞医药或其控制的主体】27日讯,前沿生物公告,公司与多瑞医药达成投资意向,拟将上海建瓴70%股权转让给多瑞医药或其控制的主体。上海建瓴持有四川前沿100%股权,四川前沿为公司在四川省成都市金堂县投资建设的高端多肽原料药生产基地。本次交易不构成关联交易,也不构成重大资产重组。交易方案及对价尚需对标的公司进行全面的财务审计、资产评估工作后由双方协商确定。后续若双方就本次交易正式签订股权转让协议,还需按照法律法规的要求履行相应的审议决策程序以及有权监管机构的审批(若涉及)。
2024-06-24 14:50
【HIV预防药成功率为100%,利空治疗药?艾迪药业回应:存量患者需要用药】6月20日,吉利德科学宣布,关键的3期PURPOSE 1临床试验中期分析顶线结果显示,每年给药两次的注射用HIV-1衣壳抑制剂lenacapavir(来那卡帕韦)在针对顺性别女性的HIV预防研究中展示出100%的有效性。6月24日,A股艾滋病药物上市公司股价大跌,截至早盘收盘,艾迪药业跌超10%,前沿生物跌近5%。对此,记者以投资者身份致电艾迪药业,相关人士表示,吉利德科学为高危暴露人群做艾滋病事前的预防,而公司为艾滋病患者做临床试验提供药物。问及未来不会有艾滋病患者时,上述人士表示,按照目前的试验结果,它可能做一定的预防,但还有大量的存量患者需要用药。(21财经)
2024-06-24 09:27
【竞价看龙头】6月24日电,市场焦点股索菱股份(5板)低开5.63%,化纤股南京化纤(3板)竞价跌停,车路云概念股华蓝集团(创业板3天2板)高开9.87%、龙元建设(3天2板)高开1.77%、日上集团(4天2板)平开,基建板块美丽生态(2板)竞价涨停、西藏天路(3天2板)平开、正平股份(3天2板)高开1.79%,医药股南华生物(2板)低开5.96%、前沿生物(科创板首板)低开1.37%,创投+芯片的力合科创(2板)低开1.86%。
2024-06-21 09:43
【创新药板块震荡拉升 前沿生物20CM涨停】6月21日电,创新药板块震荡拉升,前沿生物20CM涨停,金凯生科涨超10%,博腾股份、圣诺生物、华海药业等跟涨。消息面上,当地时间周四(6月20日),美国生物制药公司吉利德科学在官网宣布,其研发的“Lenacapavir”(来那卡帕韦)在预防艾滋病毒方面显示出了100%的有效性。
2024-05-08 20:42
【青松股份:广东可普睿生物科技有限公司相关合成生物技术尚处于前期研发阶段】青松股份5月8日在互动平台表示,广东可普睿生物科技有限公司主要专注于合成生物技术研发及新材料技术研究。公司对广东可普睿生物科技有限公司的投资控股将有助于提升其在前沿生物技术创新方面的能力,加速其在化妆品高端原料领域的布局。据悉,目前广东可普睿生物科技有限公司的相关技术尚处于前期研发阶段,尚未带来实质性收入,但不会对公司的短期经营产生影响。
2024-01-22 20:43
【前沿生物:预计2023年亏损3.1亿元—3.36亿元 同比减亏】前沿生物(688221)1月22日晚间公告,预计2023年度归属于上市公司股东的净利润将亏损3.1亿元至3.36亿元,相比之前减少约2076.41万元至4676.41万元,主要是因为营收增长和研发费用下降。2023年度,公司的营业收入主要来自抗HIV创新药艾可宁(通用名:艾博韦泰)的销售收入,预计2023年度实现的营业收入约为1.1亿元到1.15亿元,同比增加29.81%到35.71%。
2023-10-30 19:59
【前沿生物:公司及子公司通过美国FDA现场检查】10月30日晚间,前沿生物(688221)发布公告称,该公司及其全资子公司四川前沿近日接到美国食品药品监督管理局(FDA)的现场检查报告。报告显示,FB4001(特立帕肽注射液)的批准前现场检查结果为0-483通过,即无需进行任何整改。此次FDA的现场检查结果为FB4001的ANDA申请奠定了GMP合规基础,并有利于推进其在美国的ANDA审评工作进程。FB4001是公司的仿制药产品,主要用于治疗绝经后妇女及男性骨质疏松症患者,同时也适用于糖皮质激素相关的骨质疏松症患者。
2023-07-26 16:47
【前沿生物:预计上半年净亏损1.73亿元】前沿生物公告,公司预计2023年半年度归属于上市公司股东的净利润约亏损17,308.44万元,其中投入研发费用约11,192.72万元;归属于上市公司股东的扣除非经常性损益的净利润约亏损18,694.02万元。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- KDJ指标的实战智慧:超级牛散的绝密策略揭秘
- 揭秘股市成交量的秘密与操盘技巧
- K线智慧:揭秘正三角形形态的交易策略
- 股市赢家的25个成功特质
- 上市公司财务造假六宗罪:深度剖析与防范策略
- 股市智慧:深度解析止损的三重境界与实战策略
- A股市场演变与价值投资新视角
- 揭秘股市操盘艺术:深入解析主力吸筹策略
- 揭秘民间牛散八大看盘秘技:股市高手的操盘心法
- 炒股之道:超越软件与指标的深层逻辑与心理博弈
- 操盘高手揭秘:精准选股七大法则与实战心得
- 股票操作的精髓:介入节点与卖点策略的动态平衡
- 炒股心法:战胜心魔,洞悉股市真谛
- 股市智慧:掌握出货六大黄金策略
- 揭秘证券市场内幕交易四大诡异现象
- 揭秘股市真相:成交量——洞悉市场脉搏的关键指标
- 股市逆势盈利策略:精准捕捉机遇,稳健驾驭风险
- 主力底部操盘深度剖析:识破空头陷阱,洞悉建仓策略
- 精准换股:掌握九大策略,主动性解套的艺术
- 操盘手的智慧:九大生存准则深度剖析
当前版本:V3.0

 VIP复盘网
VIP复盘网
