
扫码关注公众号

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
博瑞医药
688166 |
1.33%
|
最新:54.94
开盘:55.19 昨收:54.22 |
开盘%:1.79%
振幅%:4.78% 换手%:1.39% |
最高:56.49
最低:53.9 量比:0.71 |
总市值:232 亿
流通值:232 亿 成交额:4 亿 |
- 基本信息
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
- 分时图
- 日K图
- 周K图
- 月K图
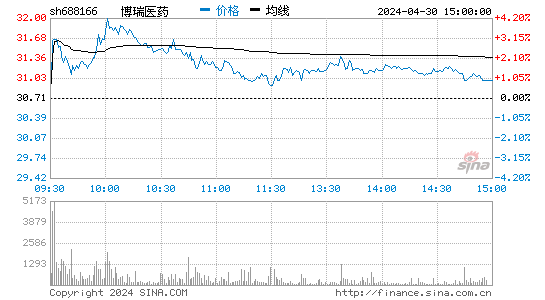
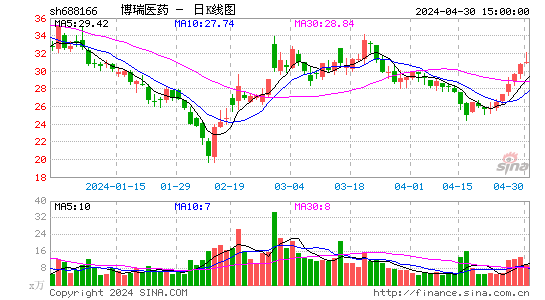
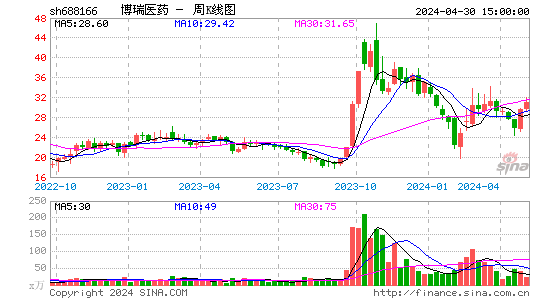
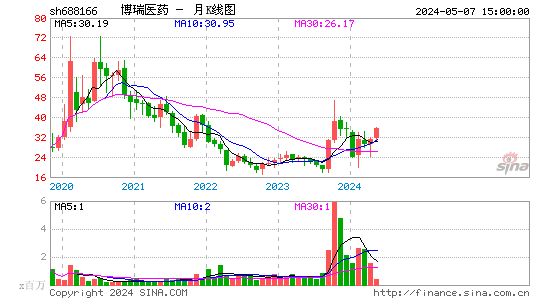
博瑞医药股票概况
深入解析博瑞医药及其股市表现
公司概况
博瑞医药成立于多年前,自创立以来,始终秉持创新、品质、服务的核心价值观,致力于成为全球领先的医药企业。公司总部位于中国,并在国内外设有多个研发和生产基地。
业务领域
仿制药领域:博瑞医药在高端仿制药领域具有深厚的技术积累。公司专注于复杂制剂的研发和生产,包括缓控释制剂、透皮制剂、脂质体等,为市场提供了多个优质仿制药产品。
创新药领域:在创新药研发方面,博瑞医药同样表现出色。公司拥有一支专业的研发团队,致力于新药发现、临床前研究及临床试验等各阶段的工作。
研发实力
博瑞医药注重研发投入,建立了完善的研发体系。公司拥有一支高素质的研发团队,配备了先进的研发设备和实验室。
股市表现
近年来,博瑞医药的股市表现较为稳健。随着公司业务的不断拓展和盈利能力的持续提升,其股价也呈现出稳步增长的趋势。
总结:
博瑞医药作为一家专注于高端仿制药和创新药研发的上市公司,凭借其强大的研发实力和卓越的产品质量,在医药市场上取得了显著成绩。同时,其股市表现也备受投资者关注。未来,随着公司业务的不断拓展和市场竞争力的持续提升,博瑞医药有望在全球医药市场上占据更加重要的地位。
2025-06-24 13:45
【博瑞医药发布双靶点受体激动剂BGM0504 II期积极数据】6月24日,记者从博瑞医药处获悉,在美国糖尿病协会(ADA)第85届科学会议上,该公司公布了其自主研发的胰高血糖素样肽-1受体(GLP-1R)/葡萄糖依赖性促胰岛素多肽受体(GIPR)双靶点激动剂BGM0504的两项II期临床研究数据。两项独立的BGM0504 II期研究分别显示,该药物在2型糖尿病患者中表现出良好的降糖疗效,并初步显示出优于司美格鲁肽的临床疗效;同时,在超重/肥胖非2型糖尿病成人群体中,展现出显著的体重管理潜力和代谢风险指标综合获益的潜质。(记者 黄华)
2025-06-16 10:38
【化学制药板块震荡反弹,通化金马、永安药业等多股涨停】化学制药板块震荡反弹,通化金马、永安药业、*ST赛隆、北大医药、广生堂涨停,悦康药业、昂利康、复旦张江、博瑞医药、翰宇药业、仟源医药等跟涨。
2025-06-12 18:59
【博瑞医药:拟以2000万元认购苏州极客基因科技有限公司新增注册资本】12日讯,博瑞医药(688166.SH)公告称,公司拟以2000万元认购苏州极客基因科技有限公司新增注册资本,增资后将取得极客基因4.1667%股权。此次交易构成关联交易,未构成重大资产重组。
2025-06-12 13:20
【创新药概念再度拉升 百济神州涨超7%创历史新高】6月12日电,午后创新药概念再度拉升,百济神州涨超7%,再创历史新高,此前奥赛康涨停,荣昌生物、睿智医药、博瑞医药涨超10%,海思科、舒泰神、万邦德等多股涨超5%。消息面上,今日记者获悉,港股创新药企中国生物制药在第46届高盛全球医疗健康年会上透露,今年将至少有1个重量级的out-license交易落地。该股受此消息刺激大涨超15%,总市值突破1000亿港元。
2025-06-12 13:15
创新药概念午后拉升,奥赛康涨停,博瑞医药、睿智医药涨超10%,海思科、长春高新、微芯生物、舒泰神等涨幅居前
2025-06-09 09:48
【化学制药板块持续走高,罗欣药业等多股涨停】化学制药板块持续走高,罗欣药业、昂利康、易明医药、美诺华涨停,海辰药业、常山药业、海创药业-U、新天地、万邦德、博瑞医药等跟涨。
2025-05-22 15:53
博瑞医药:子公司获得碘普罗胺注射液药品注册证书。
2025-03-17 16:02
博瑞医药:硫酸艾沙康唑原料药获得上市申请批准通知书
2025-01-06 15:48
博瑞医药:盐酸多巴胺原料药获得上市申请批准通知书
2024-12-23 16:43
博瑞医药:磺达肝癸钠注射液获得美国FDA批准。
2024-12-04 16:19
博瑞医药:BGM0504注射液降糖适应症获得Ⅲ期临床试验伦理批件
2024-12-03 16:17
博瑞医药:子公司获得“地诺孕素片”《药品注册证书》、“地诺孕素”及“重酒石酸去甲肾上腺素”《化学原料药上市申请批准通知书》
2024-10-21 16:26
【博瑞医药:BGM0504注射液减重适应症获得Ⅲ期临床试验伦理批件】21日讯,博瑞医药公告,全资子公司博瑞新创自主研发的BGM0504注射液减重适应症的Ⅲ期临床研究方案通过了牵头医院北京大学人民医院伦理审查委员会的审批,获得了《北京大学人民医院伦理审查委员会伦理审查批件》。
2024-10-13 16:20
【博瑞医药:BGM0504注射液减重适应症Ⅱ期临床试验达成预期目标】博瑞医药公告,全资子公司博瑞新创自主研发的BGM0504注射液治疗非糖尿病的超重或肥胖的Ⅱ期临床试验达成预期目标。这为BGM0504注射液后续临床研究提供了数据支持和参考,但最终的减重疗效还需要后续大样本量上中国非糖尿病的超重或肥胖受试者Ⅲ期确证性临床研究来进一步确认。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 股市高手的十年智慧结晶:解锁成功交易的钥匙
- 把握牛市起涨的黄金机遇:策略与心态并重
- 涨停板股投资的艺术:策略、风险与机遇
- 揭秘PMI:股市“风向标”的真相与挑战
- 揭秘股市雷区:七大类型股票碰不得
- 揭秘空头陷阱:炒股高手教你如何识别与应对
- 短线选股的核心要素解析
- 股市逃顶秘籍:精准捕捉清仓信号
- 散户炒股的智慧:克服通病,掌握交易法则
- KDJ指标的深度解析与实战策略
- MACD双叉陷阱的深度剖析与实战破解策略
- 涨停回马枪战术深度解析与实战应用
- 现金流量:企业经营的隐形生命线
- 股票定价的艺术:深入解析现金流贴现法
- 揭秘股市主力运作:从建仓到拉升的全面解析
- 通过量价形态洞悉个股分时承接强弱
- 揭秘股市低吸高抛之竞价图策略实战解析
- 揭秘股市操盘手法:如何运用量柱稳赚?
- 深度套牢后的智慧解套策略:从被动到主动的转变
- 市场周期的奥秘:深入剖析启动至再启动的循环过程
当前版本:V3.0

 VIP复盘网
VIP复盘网
