
扫码关注公众号
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
翰宇药业
300199 |
-1.02%
|
最新:15.5
开盘:15.59 昨收:15.66 |
开盘%:-0.45%
振幅%:8.37% 换手%:16.72% |
最高:16.54
最低:15.23 量比:1.36 |
总市值:137 亿
流通值:109 亿 成交额:7 亿 |
- 基本信息
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- Deepseek分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
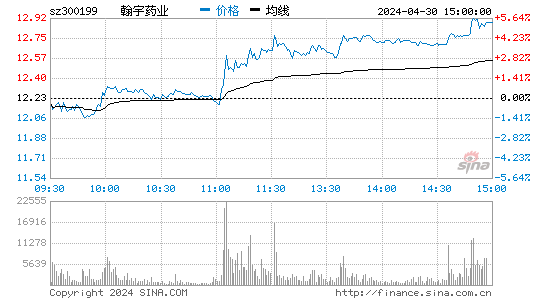
- 分时图
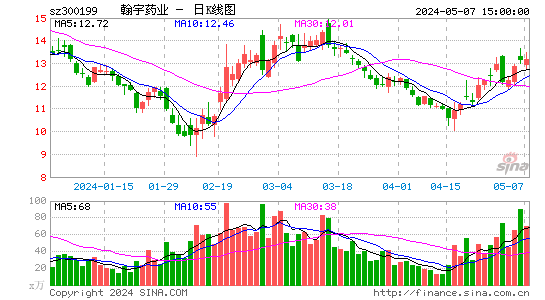
- 日K图
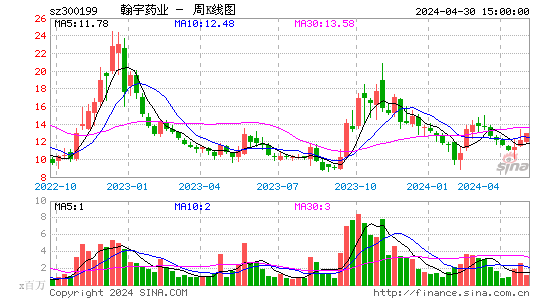
- 周K图
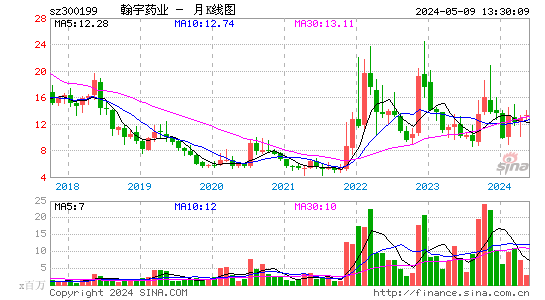
- 月K图
翰宇药业股票概览
探索翰宇药业的股市表现与公司实力
公司概况
翰宇药业是一家专注于多肽药物研发、生产和销售的高新技术企业。自成立以来,公司致力于推动多肽药物领域的技术创新和市场拓展,逐步构建起强大的研发和生产能力。
业务领域
多肽药物研发:翰宇药业在多肽药物研发领域具有深厚的积累,其研发管线涵盖了多个治疗领域,包括肿瘤、心血管、抗病毒等。
药物生产和销售:公司拥有完善的生产和销售体系,能够确保产品在全国范围内的高效供应。
财务表现
翰宇药业在财务方面表现稳健,近年来收入和利润均保持稳定增长。其盈利能力较强,为投资者提供了稳定的回报。
未来发展
翰宇药业将继续深化在多肽药物领域的研发,拓展新的治疗领域和市场。
总结:
翰宇药业作为一家专注于多肽药物研发和销售的企业,凭借其强大的研发实力和完善的销售网络,在市场中占据了一席之地。未来,随着新药的不断推出和市场的不断拓展,翰宇药业有望继续保持稳健的发展态势。
总结文字:翰宇药业在多肽药物领域具有显著的研发实力和市场竞争力,其股票在市场中备受关注。随着公司业务的不断拓展和技术的持续创新,翰宇药业有望成为多肽药物领域的领军企业。
2025-03-26 20:39
翰宇药业:预计第一季度净利润6,000万元–7,200万元,上年同期亏损1.4亿元;2024年12月23日,公司向美国食品药品监督管理局申报的利拉鲁肽注射液获得批准证书,公司此前与海外客户签署的多肽制剂及原料药等多个重要订单陆续完成发货,并在本期完成相关会计科目的确认,实现公司本期营业收入的增长
2025-02-16 17:23
【华为技术团队再度到访翰宇药业 共探AI制药新机遇】据翰宇药业消息,2月14日,华为公司技术团队再度到访翰宇药业,双方就AI制药领域的前沿技术与应用前景展开深入交流,共同探索AI与制药结合的广阔发展空间。在交流中,华为技术团队与翰宇药业研发骨干重点围绕华为云盘古药物分子大模型在多肽药物研发中的应用细节展开研讨。(证券时报)
2024-12-24 16:56
翰宇药业:利拉鲁肽注射液获得美国FDA批准证书。
2024-12-05 18:57
【翰宇药业:与DS3签订1.02亿元GLP-1原料药供应协议】12月5日电,翰宇药业公告,公司与DS3签订《产品供应协议》,DS3拟向公司采购价值约1400万美元(折合人民币约1.02亿元)的GLP-1原料药。
2024-12-04 18:39
【翰宇药业:再次收到Hikma的利拉鲁肽注射液采购需求订单】翰宇药业公告,12月3日,公司再次收到美国合作方Hikma的采购需求订单,Hikma拟向公司采购金额为1056.24万美元(约合人民币0.77亿元,含税)的利拉鲁肽注射液(仿制药)。截至本公告披露日,公司与Hikma累计签署合同金额约为3.38亿元(含税),占2023年经审计总收入的78.33%,占2023年经审计海外业务的301.14%。
2024-12-04 18:25
【翰宇药业:再次收到Hikma的利拉鲁肽注射液采购需求订单】12月4日电,翰宇药业公告,公司再次收到美国合作方Hikma的采购需求订单,Hikma拟向公司采购金额为1056.24万美元(约合人民币0.77亿元,含税)的利拉鲁肽注射液(仿制药)。截至本公告披露日,公司与Hikma累计签署合同金额约为3.38亿元。
2024-11-13 18:19
【翰宇药业:原董事袁建成挪用资金罪终审裁定 被判处有期徒刑三年六个月】11月13日电,翰宇药业公告,公司原董事、高级管理人员袁建成犯挪用资金罪一案,已收到广东省深圳市中级人民法院的终审裁定。袁建成非法挪用公司资金1685万元,被判处有期徒刑三年六个月。该案已审结。袁建成所涉犯罪行为发生在六年前,且其已于2019年8月从公司离职。公司已根据相关会计准则计提了相关费用。
2024-10-17 18:20
【翰宇药业:Hikma拟向公司采购约8400万元利拉鲁肽注射液】10月17日电,翰宇药业公告,公司收到美国合作方Hikma的采购需求订单,其拟向公司采购金额为1173.60万美元(约合人民币0.84亿元(含税))的利拉鲁肽注射液(仿制药)。
2024-10-17 10:17
医药板块异动拉升,常山药业涨超8%,翰宇药业、百花医药等跟涨(开盘啦快讯)
2024-10-14 16:20
【翰宇药业:利拉鲁肽注射液获受理】10月14日电,翰宇药业公告,公司于2024年10月12日收到国家药品监督管理局签发的利拉鲁肽注射液《受理通知书》。本品用于成人2型糖尿病患者控制血糖,适用于单用二甲双胍或 磺脲类药物最大可耐受剂量治疗后血糖仍控制不佳的患者,与二甲双胍或磺脲类药物联合应用。
2024-09-25 20:03
【翰宇药业:司美格鲁肽原料药获得DMF备案号】9月25日电,翰宇药业公告,公司收到美国食品药品监督管理局(FDA)的确认,公司司美格鲁肽原料药获得DMF(Drug Master File)备案号。
2024-09-18 16:56
【翰宇药业:艾塞那肽注射液获批上市】9月18日电,翰宇药业公告,公司艾塞那肽注射液获得国家药品监督管理局批准上市,规格分别为5μg和10μg,包装规格为1支/盒,3支/盒。艾塞那肽为GLP-1类似物,用于改善2型糖尿病患者的血糖控制。
2024-09-06 14:24
【翰宇药业:司美格鲁肽注射液减重三期临床研究方案近日公示】9月6日电,翰宇药业9月5日接受机构调研时公布司美格鲁肽临床进展:公司司美格鲁肽注射液减重三期临床研究方案,于2024年9月2日,在“药物临床试验登记与信息公示平台”首次公示,登记号CTR20243301,是国内首个在体重管理适应症上进入III期临床的司美格鲁肽注射液。试验主要目的是以原研司美格鲁肽注射液(诺和盈®)为对照,评价翰宇药业生产的司美格鲁肽注射液(HY310注射液)辅助生活方式干预治疗肥胖患者的有效性,目标入组人数408人。
2024-09-04 16:24
翰宇药业:公司的生长抑素原料药收到欧洲药品质量管理局签发的CEP证书(原料药欧洲药典适用性证书),为公司的生长抑素原料药进入欧盟市场开拓了准入通道
2024-07-18 16:55
翰宇药业:控股子公司翰宇大理向地方部门发起延期申请后通过了公安局现场复评检查,最终取得换发《云南省工业大麻加工许可证》。
2024-07-18 16:44
【翰宇药业:控股子公司通过复评换发工业大麻加工许可证】翰宇药业(300199)于7月18日晚间发布公告,宣布旗下控股子公司翰宇大理通过了公安局的现场复评检查,成功取得换发《云南省工业大麻加工许可证》。此次获得许可证将助力公司在国内实现工业大麻深加工业务的合法发展,稳步推进公司的长期稳定发展。
2024-07-15 20:58
【翰宇药业:控股股东、实控人拟向深圳担保集团非交易过户合计2.26%股份】翰宇药业公告,公司控股股东、实际控制人曾少贵、曾少强拟分别将其持有的1.26%、1.00%股份非交易过户给深圳担保集团有限公司。本次非交易过户金额全部用于偿还股票质押融资本息。
2024-07-10 19:15
【翰宇药业:子公司签订约5889万元GLP-1原料药供应合同】7月10日电,翰宇药业公告,全资子公司翰宇药业(武汉)有限公司收到客户DS3 RX LLC的合作协议,其拟向翰宇武汉采购金额约810万美元(约合人民币5889万元(含税))的GLP-1原料药。
2024-07-04 16:27
【翰宇药业:注射用特利加压素获得智利批准证书】7月4日电,翰宇药业公告,公司近日收到智利国家药品管理局颁发的关于注射用特利加压素的批准证书,标志着公司拥有了在南美部分市场的销售该药品的资格,为公司国际市场业务的开拓带来更多机会。
2024-07-03 18:08
【翰宇药业:原董事袁建成犯挪用资金罪 被判处有期徒刑三年六个月】7月3日电,翰宇药业公告,公司近日收到广东省深圳市南山区人民法院出具的《刑事裁定书》,公司原董事、高级管理人员袁建成犯挪用资金罪已经广东省深圳市南山区人民法院判决。袁建成犯挪用资金罪,被判处有期徒刑三年六个月。
2024-07-01 16:31
【翰宇药业:全资子公司鲑降钙素原料药获得上市申请批准通知书】翰宇药业公告,全资子公司翰宇武汉收到国家药品监督管理局签发的关于鲑降钙素原料药《化学原料药上市申请批准通知书》,鲑降钙素是调节钙代谢,抑制甲状旁腺的激素之一,它能显著地降低高周转性骨病的骨钙丢失。
2024-06-27 20:58
【翰宇药业:公司替尔泊肽原料药已启动出口海外减肥市场的计划】6月27日电,翰宇药业在互动平台表示,6月27日,公司替尔泊肽原料药收到美国食品药品监督管理局(FDA)DMF备案号,在同品种的市场竞争中,取得DMF注册登记号的企业和其产品容易被客户优先考虑,有利于企业寻找市场机遇、开拓客户。未来,该备案可在相关药物申报中被直接引用,从而节约产品审查和评估时间,加速项目申报获批进程。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 掌握DDZ指标,精准捕捉股市大单动向
- 股市风云录:掌握“四忌五不”,智胜股市波动
- 揭秘股市主升浪:掌握简便炒股技巧,精准捕捉盈利时机
- 如何精准捕捉个股筑底反弹信号
- MACD与KDJ的协同作战:揭秘牛散连续捕获涨停的策略
- KDJ指标的深度解析与实战应用
- MACD金叉的多样性与实战应用
- 掌握股市动脉:快速看盘的五大关键技巧
- 三招制胜:揭秘高效选股策略
- 股市追涨策略深度解析:精准捕捉涨停板时机
- 羽绒服市场的繁荣与技术、品牌及产业链的共赢
- 识别下跌中继平台:精准把握股市脉搏的三把钥匙
- 短线交易的盈利迷思与资金管理策略探索
- 波浪理论深度解析:洞察市场波动的秘密
- 从下岗到财务自由:我的职业炒股之路
- 八招制胜法则,深度解析A股投资策略
- 警惕股市暗礁:识别与规避价值陷阱的艺术
- 现金流量表:洞察绩优公司的财务密钥
- DMI指标:精准捕捉市场动向的利器
- 如何精准选出长线好股票
当前版本:V3.0

 VIP复盘网
VIP复盘网
