
扫码关注公众号
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
信立泰
002294 |
0.06%
|
最新:33.86
开盘:33.82 昨收:33.84 |
开盘%:-0.06%
振幅%:2.07% 换手%:0.65% |
最高:34.21
最低:33.51 量比:0.77 |
总市值:377 亿
流通值:377 亿 成交额:11 亿 |
- 基本信息
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- Deepseek分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
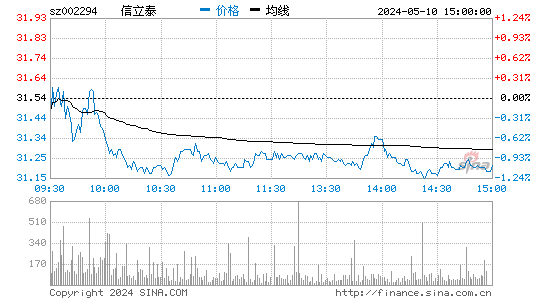
- 分时图
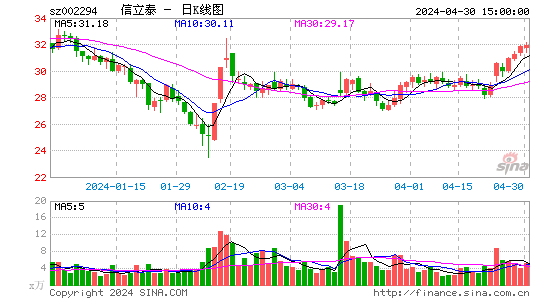
- 日K图
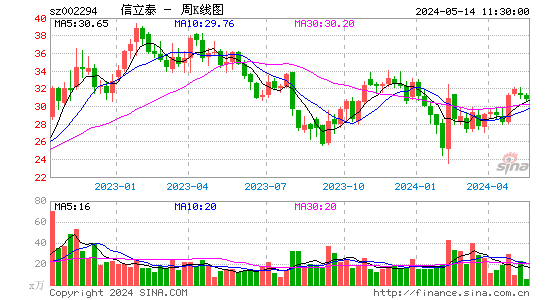
- 周K图
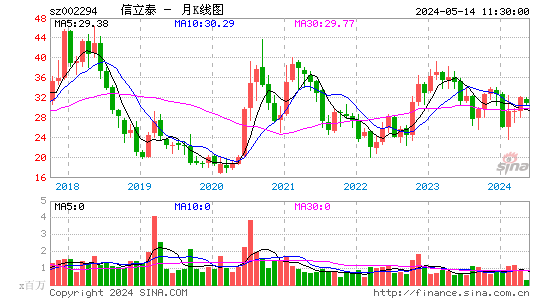
- 月K图
信立泰股票概况
全面了解信立泰股票及其公司背景
公司概况
信立泰药业股份有限公司是一家专注于心血管、抗肿瘤、降血糖等重大疾病领域的医药企业。公司自成立以来,凭借强大的研发实力和丰富的产品线,赢得了市场的广泛认可。
业务领域
信立泰在心血管领域有着深厚的技术积累,推出了一系列创新药物。同时,公司还积极拓展抗肿瘤、降血糖等其他重大疾病领域,形成了多元化的产品结构。
财务状况
近年来,信立泰的财务表现稳健。随着业务的不断拓展和市场份额的提升,公司的盈利能力持续增强。投资者对信立泰的未来发展充满信心。
未来发展
展望未来,信立泰将继续加大研发投入,推动更多创新药物的上市。同时,公司还将积极寻求外部合作,拓展国内外市场,实现业务的持续增长。
总结
信立泰作为医药行业的佼佼者,凭借强大的研发实力和多元化的产品结构,在市场中占据了一席之地。投资者对信立泰股票的前景持乐观态度。
2025-03-24 11:04
【深圳:政企医联动,共谋罕见病医药发展创新】3月20日上午,深圳市发展改革委(市药械办)联合市卫生健康委、市医保局,在河套深港科技创新合作区信立泰创新药发现中心召开“罕见病药院企座谈会”。会议汇聚政府、医院、企业三方力量,共谋罕见病诊疗生态建设,推动政策、临床与研发深度协同。接下来,深圳市将从资金支持、临床试验、用药支付等三个方面发力,努力克服罕见病药物研发多重挑战,持续推动罕见病药物在我市差异化布局和取得更多实效,致力打造全球罕见病防治标杆城市。(证券时报)
2025-02-13 17:31
信立泰:SAL0140药品临床试验申请获得受理
2025-01-20 15:48
信立泰:JK07在HFrEF(射血分数降低的心衰)和HFpEF(射血分数保留的心衰)患者的MRCT II期临床试验中获得积极的中期数据。
2025-01-20 15:44
【信立泰:JK07境外临床试验取得积极中期数据】1月20日电,信立泰公告,公司收到子公司Salubris Bio通知,JK07在HFrEF和HFpEF患者的MRCT II期临床试验中获得积极中期数据。JK07的II期临床研究中期分析旨在评估其在低剂量组(0.045mg/kg)的安全性,为启动高剂量组(0.09mg/kg)提供保障。根据中期分析结果,已启动高剂量组的患者入组。JK07的II期临床试验为随机、双盲、安慰剂对照、剂量递增研究,旨在评估其在HFrEF和HFpEF患者中的安全性和有效性。试验计划纳入282例心衰患者,本次中期分析纳入了最初随机的68名患者。数据显示,JK07在低剂量组中显示出良好的安全性和耐受性,两组在不良事件的发生频率和严重性方面无显著差异,并初步观察到积极疗效信号。JK07是公司自主研发、具有全球知识产权的NRG-1融合抗体药物,是心衰领域首个进入临床开发阶段的抗体融合蛋白、选择性ErbB4激动剂,拟开发适应症包括HFrEF和HFpEF。
2024-11-28 16:00
信立泰:阿利沙坦酯氨氯地平片(复立坦)、苯甲酸福格列汀片(信立汀)新纳入国家医保目录。
2024-10-21 18:40
【信立泰:拟3.5亿元增资控股子公司Salubris Bio】10月21日电,信立泰公告称,公司拟以自筹资金5,000万美元(约合人民币3.5亿元)向其位于美国的创新生物制药研发中心Salubris Bio增资。增资完成后,公司对Salubris Bio的投资总额将增至约人民币13.22亿元,Salubris Bio仍为公司控股子公司。增资款计划主要投向JK07、JK06的临床研究,以及Salubris Bio平台建设和研发管线的布局等。本次增资符合子公司业务发展的实际需要,符合公司发展战略和长远规划。
2024-08-05 15:52
【信立泰:抗肿瘤药JK06获批欧洲I期临床】8月5日电,信立泰公告,公司子公司SalubrisBio自主研发的广谱抗肿瘤创新生物药JK06已获批可在欧洲部分国家开展I期临床研究。
2024-07-31 19:01
【信立泰:恩那度司他新适应症获得临床试验批准通知书】信立泰(002294)7月31日晚间公告,近日,公司收到国家药监局核准签发的《临床试验批准通知书》,同意公司的恩那度司他片开展新适应症(治疗非髓系恶性肿瘤患者化疗引起的贫血,简称“CIA”)的临床试验。
2024-07-30 20:14
【信立泰:SAL0120获得临床试验批准通知书】信立泰(002294)7月30日晚间公告,近日,公司收到国家药监局核准签发的《临床试验批准通知书》,同意公司自主研发的创新小分子药物SAL0120片(项目代码:SAL0120)开展治疗慢性肾脏病(CKD)的临床试验。
2024-07-05 15:58
【信立泰:苯甲酸福格列汀片(信立汀)获得药品注册证书】7月5日电,信立泰公告,近日,公司收到国家药品监督管理局核准签发的苯甲酸福格列汀片(商品名:信立汀)药品注册证书。苯甲酸福格列汀片(信立汀)是一种二肽基肽酶4(DPP-4)抑制剂,用于改善成人2型糖尿病患者的血糖控制。
2024-06-25 16:12
【信立泰:SAL056上市申请获受理】6月25日电,信立泰公告,子公司信立泰(苏州)药业有限公司的生物药“注射用特立帕肽”(SAL056)申报上市申请获得国家药品监督管理局受理。SAL056是长效骨形成促进剂,每周一次皮下注射,拟用于治疗有骨折高发风险的绝经后妇女骨质疏松症。目前国内尚无同规格及用法用量的产品。若获批上市,将大幅提高患者用药便利性。
2024-05-21 18:00
信立泰:阿利沙坦酯氨氯地平片(复立坦)获得药品注册证书
2024-04-07 16:27
【信立泰:JK07获得境内临床试验批准通知书】4月7日电,信立泰公告,近日,公司、美国SalubrisBio收到国家药品监督管理局核准签发的《药品临床试验批准通知书》,同意JK07注射液开展治疗成人慢性心力衰竭(RENEU-HF)的II期临床试验。
2024-03-25 19:50
【信立泰:2023年净利同比降8.95% 拟10派5元】3月25日电,信立泰公告,2023年实现营业收入33.65亿元,同比下降3.35%;净利润5.8亿元,同比下降8.95%;基本每股收益0.52元。公司拟每10股派发现金红利5元(含税)。
2023-12-13 19:27
信立泰:阿利沙坦酯片(信立坦)、恩那度司他片(恩那罗)纳入国家医保目录
2023-12-13 19:19
【信立泰宣布 阿利沙坦酯片(信立坦)和恩那度司他片(恩那罗)已被纳入国家医保目录】信立泰宣布,阿利沙坦酯片(信立坦)和恩那度司他片(恩那罗)已被纳入国家医保目录。
2023-11-22 16:29
【信立泰:子公司可以开展JK07慢性心力衰竭的HFrEF和HFpEF适应症的II期临床研究】11月22日电,信立泰公告,公司收到子公司美国Salubris Bio的通知,根据相关规则,可以在美国开展JK07慢性心力衰竭的HFrEF(射血分数降低的心衰)和HFpEF(射血分数保留的心衰)适应症的II期临床研究。目前SalubrisBio提交有关申请已届满30日,根据有关规定可以开展JK07慢性心力衰竭的HFrEF和HFpEF适应症的II期临床研究。
2023-11-19 14:34
【2023国谈第三日下午场开幕!晖致、贝达、信立泰、基石药业首轮被点名】《科创板日报》11月19日讯,2023年医保国谈第三日下午场在相对轻松的氛围中拉开序幕,首轮多家企业被点名,包括但不限于晖致、贝达、信立泰、基石药业等企业。据悉,这些企业均涉及创新药产品。在下午场开启前,便有前来确认地点的企业人员向记者透露,参加的是肿瘤创新药的续约谈判,之前进过2次了。由此猜测,下午的谈判重点或围绕肿瘤创新药展开。(蓝鲸记者 郑炳巽)
2023-10-17 16:09
【信立泰:沙库巴曲缬沙坦钠片获得药品注册证书】信立泰公告,近日,公司收到国家药监局核准签发的“沙库巴曲缬沙坦钠片”药品注册证书,并视同通过仿制药一致性评价。该产品用于射血分数降低的慢性心力衰竭(NYHAⅡ-Ⅳ级,LVEF≤40%)成人患者,降低心血管死亡和心力衰竭住院的风险;以及治疗原发性高血压。
2023-10-17 16:01
信立泰:沙库巴曲缬沙坦钠片获得药品注册证书
2023-10-10 17:10
【信立泰:JK07治疗HFrEF的美国Ib期临床试验积极数据公布】10月10日电,信立泰公告,近日,公司收到子公司美国Salubris Bio的通知,其在美国心衰协会2023年度科学会议最新发布口头汇报专场公布了JK07治疗HFrEF(射血分数降低的心衰)的美国Ib期临床试验的积极数据。数据显示,JK07显示出良好的安全性、初步疗效,并确定了治疗安全窗。公司将在II期多次给药临床试验中进一步评估JK07在HFrEF和HFpEF(射血分数保留的心衰)患者中的疗效和安全性。JK07是公司第一个中美双报的创新生物药,目前处于I期临床试验阶段,存在一定不确定性。
2023-10-08 19:16
【信立泰:SAL0120片获得临床试验批准通知书】10月8日电,信立泰公告,公司收到国家药品监督管理局核准签发的《临床试验批准通知书》,同意公司自主研发的创新小分子药物SAL0120片(项目代码:SAL0120)开展治疗IgA肾病的临床试验申请。SAL0120是公司自主研发的小分子ETA受体拮抗剂,拟开发适应症包括IgA肾病,及轻、中度原发性高血压。目前正在开展I期临床试验。
2023-09-11 19:21
【信立泰:SAL0108上市申请获得受理】信立泰(股票代码:SAL0108)近日宣布,其上市申请已获得受理。
2023-08-24 18:56
【信立泰:半年报扣非净利润3.03亿元 同比增长6.91%】8月24日电,信立泰披露2023年半年度报告,实现营业收入16.84亿元,同比增长0.97%;归属于上市公司股东的净利润3.38亿元,同比下降3.04%;归属于上市公司股东的扣除非经常性损益的净利润3.03亿元,同比增长6.91%;基本每股收益0.300元。
2023-08-10 17:38
【信立泰:子公司腔静脉滤器系统获得医疗器械注册证】8月10日电,信立泰公告,子公司深圳市科奕顿生物医疗科技有限公司自主研发的“腔静脉滤器系统”(SaExten®)获得国家药品监督管理局的注册批准。该产品通过经股静脉或经颈静脉入路经皮置入,用于预防下腔静脉系统栓子脱落而引起的肺动脉栓塞(PE)。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 掌握高抛低吸的艺术:股市盈利的智慧之道
- 股市运行的深层动因剖析
- MACD金叉:精准捕捉股票买入信号的利器
- 京城散户厅里的股市人生:全职外婆与八旬老翁的波段传奇
- 量价收缩:精准把握买入时机的关键
- 揭秘复苏型股票的买入良机
- 炒股智慧:资深股民揭秘盈利与避坑法则
- 揭秘资金流向:如何捕捉市场金股
- DDYS指标:深化理解与应用策略
- 地量:股市中最有价值的技术指标揭秘
- 捕捉市场先机:变盘前的微妙信号与策略布局
- 股票内在价值探索:精准评估与市场智慧的融合
- 解读“三四法则”:探寻高利润投资之道
- 超级大户的A股行踪揭秘与市场风向
- 散户应对股市暴跌的全面策略:事前预防与事后应对
- 主力建仓的蛛丝马迹:深度剖析与实战策略
- 证监会强调:上市公司股东减持需严格遵守规定
- 揭秘个股跳水背后的主力意图
- 股市智慧:解锁合格股民的必备策略
- 揭秘涨停复制法:精准捕捉涨停股的艺术
当前版本:V3.0

 VIP复盘网
VIP复盘网
