
扫码体验VIP

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
万邦德
002082 |
10.01%
|
最新:8.57
开盘:8.09 昨收:7.79 |
开盘%:3.85%
振幅%:8.6% 换手%:17.77% |
最高:8.57
最低:7.9 量比:5.44 |
总市值:52 亿
流通值:47 亿 成交额:6 亿 |
- 基本信息
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
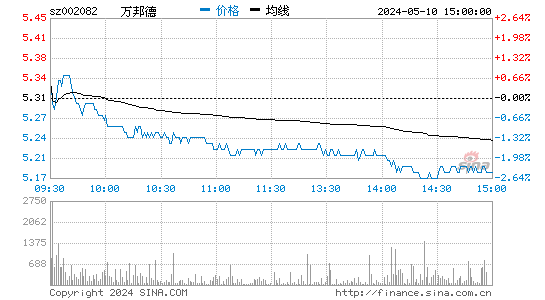
- 分时图
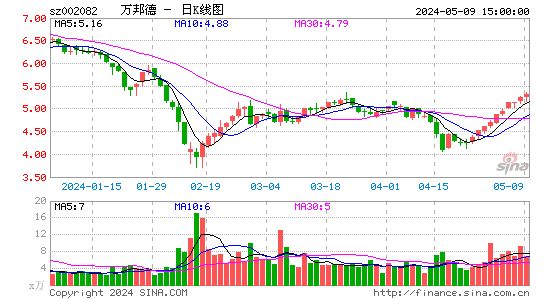
- 日K图
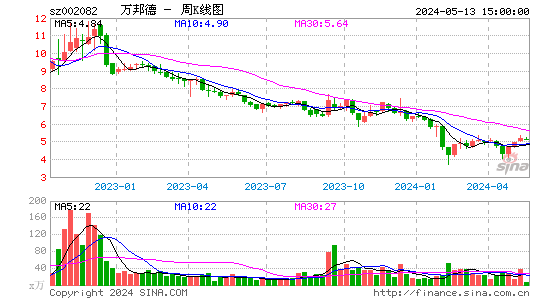
- 周K图
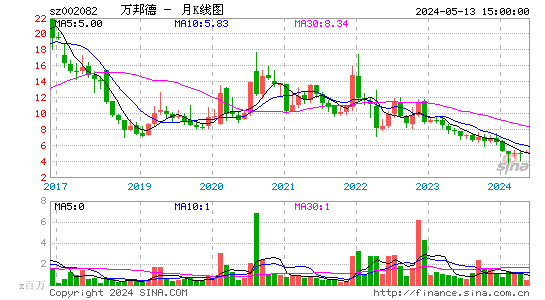
- 月K图
万邦德股票概况
全面了解万邦德及其股市表现
公司概况
万邦德是一家专注于医药健康领域的高新技术企业,致力于药品研发、生产和销售。公司拥有一支高素质的研发团队和完善的生产体系,产品涵盖多个治疗领域,具有较高的市场占有率。
业务分析
主营业务:万邦德的主营业务包括医药制造和医疗器械制造两大板块。医药制造方面,公司专注于抗生素、心脑血管等领域的产品开发;医疗器械制造则涵盖了一次性使用无菌医疗器械等多个细分领域。
市场竞争力:凭借先进的技术和优质的产品,万邦德在医药健康领域具有较高的市场竞争力。
财务表现
近年来,万邦德的财务状况稳健,营业收入和净利润持续增长。公司的盈利能力、偿债能力和运营效率均表现出色。
市场地位
作为医药健康领域的佼佼者,万邦德在市场上享有较高的知名度和美誉度。其品牌影响力日益增强,为公司的持续发展奠定了坚实基础。
总结:
万邦德是一家实力雄厚的医药健康企业,业务覆盖广泛,市场竞争力强,财务状况稳健。未来,随着医药健康市场的不断扩大和消费升级,万邦德有望迎来更加广阔的发展前景。
总结:
万邦德作为医药健康领域的领军企业,凭借其强大的研发实力、优质的产品和服务,以及稳健的财务状况,在市场上赢得了广泛的认可和赞誉。
2025-07-16 15:14
【7月16日涨停分析】今日共55股涨停,连板股总数13只,21股封板未遂,封板率为72%(不含ST股、退市股)。焦点股方面,机器人概念股上纬新材20CM6连板,创新药概念股联环药业8天6板、万邦德2连板,包装印刷板块森林包装10天8板。
2025-07-16 13:51
【创新药板块持续活跃,万邦德、哈三联午后涨停】创新药板块持续活跃,万邦德、哈三联午后封板,丽珠集团、健康元、金石亚药跟涨。
2025-07-16 13:31
【仿制药板块午后上涨 广生堂涨超12%】7月16日电,仿制药板块午后上涨,截至发稿,广生堂涨超12%,润都股份、力生制药、万邦德涨停,丽珠集团、吉华集团等跟涨。
2025-07-16 11:26
创新药概念反复活跃,广生堂涨超10%,股价创出阶段新高,润都股份、联环药业、千红制药此前涨停,万邦德、丽珠集团等涨幅居前
2025-07-14 16:06
【万邦德:子公司获得防治阿尔茨海默病、皮肤光老化的发明专利】7月14日电,万邦德(002082.SZ)公告称,公司全资子公司万邦德制药集团有限公司近日获得国家知识产权局的《发明专利证书》,发明名称为一种用于防治阿尔茨海默病、皮肤光老化的组合物、制剂及其应用。该专利首创性开发“人参-银杏叶-千层塔”的1类新药复方组合物,具有安全性高、用药剂量小、药物构成简单且疗效更好的特点。凭借多成分-多靶点-多通路的整合调节优势,形成干预阿尔茨海默病病理网络的创新疗法,为患者提供优于现有单剂制药物的治疗方案。
2025-07-11 19:27
【万邦德:控股股东等拟协议转让公司9.8089%股份】7月11日电,万邦德(002082.SZ)公告称,公司控股股东万邦德集团、实际控制人赵守明、庄惠、一致行动人温岭惠邦、温岭富邦拟通过协议转让方式,向温岭市万龙医药科技合伙企业转让其持有的公司股票合计6000万股,占公司总股本的9.8089%。转让价格为6.88元/股,股份转让总价款合计为4.128亿元。
2025-07-11 19:24
万邦德:控股股东及一致人拟向万龙医药转让其持有的公司9.8089%股份,股份转让总价款合计为人民币4.128亿元。
2025-07-07 15:53
【万邦德:WP107口服溶液药物临床试验申请获批】7月7日电,万邦德(002082)7月7日晚间公告,全资子公司万邦德制药集团有限公司于近日收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,公司自主研发的WP107口服溶液用于治疗“重症肌无力”的临床试验申请获得批准。
2025-06-30 16:56
【万邦德:子公司新药石杉碱甲控释片获伦理批件】6月30日电,万邦德(002082)6月30日晚间公告,公司全资子公司万邦德制药集团有限公司的2.2类新药石杉碱甲控释片治疗轻中度阿尔茨海默病型痴呆的关键注册临床试验近日获得了组长单位首都医科大学宣武医院伦理审查委员会的审查批件,批准项目开展。
2025-06-30 16:19
万邦德:子公司石杉碱甲控释片获得伦理批件
2025-06-12 13:20
【创新药概念再度拉升 百济神州涨超7%创历史新高】6月12日电,午后创新药概念再度拉升,百济神州涨超7%,再创历史新高,此前奥赛康涨停,荣昌生物、睿智医药、博瑞医药涨超10%,海思科、舒泰神、万邦德等多股涨超5%。消息面上,今日记者获悉,港股创新药企中国生物制药在第46届高盛全球医疗健康年会上透露,今年将至少有1个重量级的out-license交易落地。该股受此消息刺激大涨超15%,总市值突破1000亿港元。
2025-06-11 11:59
【万邦德针对新生儿缺氧缺血性脑病HIE的WP103项目立项】11日讯,近日,万邦德针对新生儿缺氧缺血性脑病HIE的WP103项目立项,该项目由北京大学第一医院儿童医学中心教授团队申请获批,双方将就WP103在HIE治疗中的药效机制展开研究,重点探索潜在疗效和安全性。
2025-06-11 10:34
创新药概念震荡调整,联化科技盘中触及跌停,万邦德、哈三联、万邦医药、舒泰神跌超5%,翰宇药业、益方生物等跟跌
2025-06-09 09:48
【化学制药板块持续走高,罗欣药业等多股涨停】化学制药板块持续走高,罗欣药业、昂利康、易明医药、美诺华涨停,海辰药业、常山药业、海创药业-U、新天地、万邦德、博瑞医药等跟涨。
2025-06-06 13:26
【创新药概念午后回暖 常山药业涨超15%创历史新高】6月6日电,创新药概念震荡回升,常山药业涨超15%,再创历史新高,迈威生物涨超10%,昂利康触及涨停,神州细胞、万邦德、新诺威、海创药业等纷纷冲高。消息面上,华福证券研报显示,2020年至2024年,创新药BD交易总金额从92亿美元提高到523亿美元,首付款金额从6亿美元提升到41亿美元。2025年初至今,创新药出海交易总金额已达455亿美元,首付款已达到22亿美元,全年有望创新高。
2025-06-06 10:15
创新药概念反复活跃,海辰药业20cm涨停,常山药业涨超14%,万邦德、海南海药、舒泰神、翰宇药业等涨幅居前
2025-06-06 10:05
【创新药概念异动 海辰药业涨超15%】6月6日电,创新药概念异动,海辰药业涨超15%,赛伦生物、常山药业涨超10%,万邦德、昂利康、圣诺生物等股拉升。
2025-06-05 09:28
【竞价看龙头】6月5日电,市场焦点股御银股份(5板)低开4.04%,深海科技概念股尤夫股份(16天8板)高开2.55%,黄金概念股莱绅通灵(11天6板)低开0.54%、菜百股份(5天3板)低开1.12%,新消费板块乐惠国际(7天5板)高开7.44%、有友食品(6天3板)低开1.44%,创新药概念股万邦德(3板)平开、九芝堂(2板)低开0.10%,体育产业的共创草坪(3板)高开9.85%、金陵体育(创业板2板)高开4.49%,商业航天概念股中衡设计(3板)高开1.85%。
2025-06-04 09:27
【竞价看龙头】6月4日电,市场焦点股百利电气(12天7板)高开9.99%,并购重组的滨海能源(11天7板)低开2.70%,无人车辆概念股德邦股份(5板)高开0.52%,新消费概念股均瑶健康(6天5板)高开5.48%、乐惠国际(6天4板)高开9.76%,化工股永冠新材(7天5板)高开7.24%、联化科技(4板)高开5.24%,数字货币概念股御银股份(4板)高开5.02%、恒宝股份(3板)高开1.53%,创新药概念股万邦德(2板)高开9.87%、海南海药(2板)竞价涨停。
2025-06-03 15:58
【6月3日连板股分析:连板股晋级率35% 创新药概念全线爆发】今日共68股涨停,连板股总数15只,其中三连板及以上个股6只,上一交易日共17只连板股,连板股晋级率35.29%(不含ST股、退市股)。个股方面,全市场超3300只个股上涨,逾百股涨超9%。高位股迎来修复,均瑶健康、合兴股份上演“地天板” ,滨海能源、永冠新材、乐惠国际、锦泓集团等走出反包行情。不过值得注意的是高度板(5连板)德邦股份午后数度炸板,另一只人气股百利电气午后同样遭遇分歧。板块方面,创新药概念继续发威,近20股涨停或涨超10%,其中人气股舒泰神触及涨停,今年以来累积涨幅超300%,万邦德、海南海药、哈三联晋级2连板;银行板块全天强势,沪农商行涨停,兴业银行涨近5%,消息面上,沪农商行将调入沪深300指数与上证180指数的样本股。
2025-06-03 09:36
【创新药概念异动拉升 华海药业等涨停】6月3日电,创新药概念异动拉升,华海药业、万邦德、海南海药涨停,冠昊生物涨逾10%,千红制药、联化科技、舒泰神等涨幅居前。
2025-04-28 15:47
万邦德:子公司WP107(石杉碱甲口服溶液)药品临床试验申请获得国家药监局受理
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 涨停板换手率:揭秘股市强弱的密码
- 揭秘股市分析利器:深入解读BOLL指标及其综合应用
- 股市智慧:掌握六大要点,解锁盈利之门
- 市场走出底部的六大信号
- 捕捉个股起涨信号,精准布局未来涨幅
- 散户炒股实战指南:掌握七大技巧,稳健盈利
- 股市解套策略:利用T+0思维与灵活操作降低成本
- 股市提款机:散户实战策略与心态调整指南
- 揭秘黑马股的交易量能密码
- 揭秘股市牛股飙升的七大秘诀
- 股市秘籍:精准捕捉盘中拉升信号
- 比率分析法:深入剖析企业财务状况的利器
- 掌握KDJ指标,精准把握股市买卖时机
- 如何规避交易中的七大陷阱,成就智慧交易者
- 高手解读:揭秘股市七大买入形态与策略
- 主力出货的千层套路:揭秘股市中的隐秘手法
- 股市资金流向的深度解析与实战应用
- 精准辨识:股市中的上涨与反弹策略
- 掌握缠论精髓,捕捉主升浪机会
- 股市投资:掌握四大法宝,稳健航行于风险之海
当前版本:V3.0

 VIP复盘网
VIP复盘网
