
扫码关注公众号

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
双鹭药业
002038 |
-1.34%
|
最新:6.64
开盘:6.73 昨收:6.73 |
开盘%:0%
振幅%:1.78% 换手%:0.83% |
最高:6.74
最低:6.62 量比:1.4 |
总市值:68 亿
流通值:57 亿 成交额:9 亿 |
- 基本信息
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
- 分时图
- 日K图
- 周K图
- 月K图
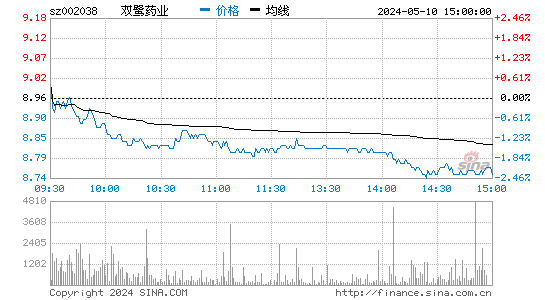
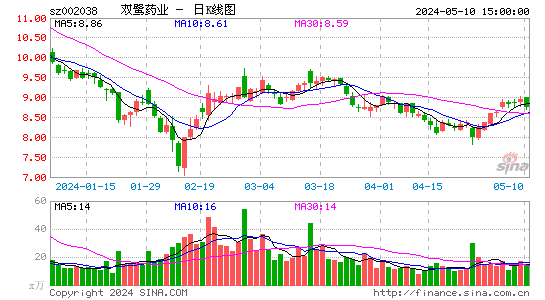
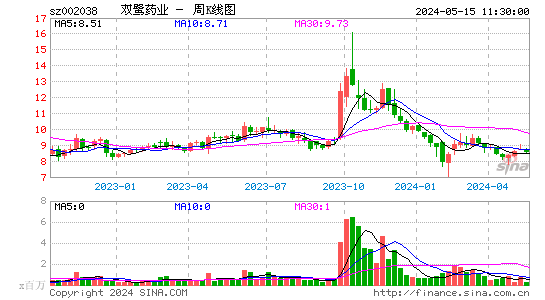
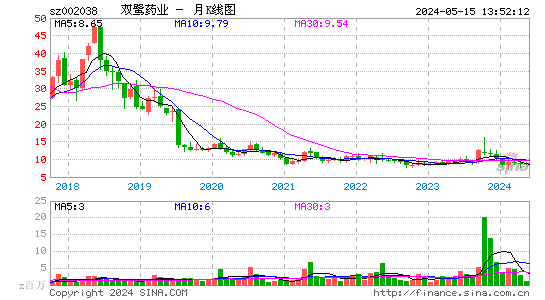
双鹭药业股票概况
全面解析双鹭药业的企业背景与市场表现
双鹭药业股票最新百科信息
双鹭药业,全称为北京双鹭药业股份有限公司,股票代码002038,是深圳证券交易所上市企业。公司成立于1994年,专注于基因工程及相关药物的研究开发和生产经营。近年来,公司总资产稳定,市场表现活跃,是医药制造领域的知名企业。
什么是双鹭药业
# 企业背景与发展历程
双鹭药业自成立以来,凭借技术优势和持续创新,已研发并投放市场包括国家一类新药在内的多个品种。公司业务覆盖肿瘤、心脑血管、肝病等多个治疗领域,拥有丰富的产品储备。
# 研发实力与创新能力
双鹭药业拥有国家级企业技术中心,下设多个研究室,拥有200余名研发人员。公司近十年研发投入占销售收入的10%以上,成功研制并推出数十种新药。此外,公司还在美国设立研发中心,推进国际化战略。
# 市场表现与财务状况
双鹭药业市场表现稳健,总资产规模庞大。截至最新数据,公司总资产超过59亿元,股东权益合计近56.4亿元。公司资产负债率较低,显示出良好的财务健康状况。
# 社会责任与行业地位
双鹭药业作为国内生物制药的骨干企业,不仅致力于技术创新和产品研发,还积极履行社会责任。公司多次获得国家和北京市科技进步奖,是行业内的佼佼者。
总结
双鹭药业凭借强大的研发实力和创新能力,在生物制药领域取得了显著成就。公司市场表现稳健,财务状况良好,是投资者值得关注的优质股票。
2025-04-08 16:47
双鹭药业:获得硝酸甘油喷雾剂药品注册证书
2025-04-01 16:39
双鹭药业:获得瑞戈非尼片药品注册证书。
2024-10-15 18:25
【双鹭药业:依替巴肽注射液获药品注册证书】双鹭药业公告,公司于近日收到国家药品监督管理局核准签发的依替巴肽注射液《药品注册证书》。该药品为特异性的血小板糖蛋白IIb/IIIa受体拮抗剂,主要用于急性冠状动脉综合征患者的介入术后抗血栓治疗等。
2024-07-05 17:15
【双鹭药业:获得硫酸氨基葡萄糖胶囊药品注册证书】7月5日电,双鹭药业公告,公司于近日收到国家药品监督管理局核准签发的硫酸氨基葡萄糖胶囊(商品名:级宁®)《药品注册证书》。本品上市将丰富公司老年慢病产品的储备,并增加公司口服固体制剂产品的储备,将促进公司电商渠道销售业务的开展,有利于提升公司的市场竞争力和品牌影响力。
2024-06-24 22:02
【双鹭药业:董事会秘书拟减持公司股份不超50.02万股】6月24日电,双鹭药业公告,公司董事、董事会秘书梁淑洁计划在3个月内以集中竞价交易方式减持公司股份不超过50.02万股(占公司总股本的比例不超过0.0487%)。
2024-06-21 19:57
【双鹭药业:拟对普乐康增资4000万元】双鹭药业公告,公司将出资4000万元参与普乐康增资。普乐康增资完成后,双鹭药业持有普乐康11.765%股权。公司后期将继续与普乐康展开战略合作,投资支持普乐康完成PHP1003项目和PHP0101项目包括临床试验和工艺验证等后续研发工作,并视项目进展和投资情况确定增持普乐康公司股权及展开项目产业化和商业化等深度合作。
2024-05-30 18:32
【双鹭药业:注射用丁二磺酸腺苷蛋氨酸通过一致性评价】5月30日电,双鹭药业公告,公司注射用丁二磺酸腺苷蛋氨酸通过仿制药质量和疗效一致性评价。注射用丁二磺酸腺苷蛋氨酸适用于肝硬化前和肝硬化所致肝内胆汁淤积及妊娠期肝内胆汁淤积。
2024-05-30 18:28
双鹭药业:注射用丁二磺酸腺苷蛋氨酸通过一致性评价
2024-01-26 20:55
【双鹭药业:2023年净利同比预增66%—100%】双鹭药业(002038)公布了1月26日晚间的业绩预告,预计2023年归母净利润将增长66%至100%,预计范围为3.9亿元至4.7亿元。报告期间,公司的非经常性损益受到持有交易性金融资产及可供出售金融资产的公允价值变动的影响较大,该影响金额在1.7亿元至2亿元之间。此外,公司的产品结构发生了变化,新上市产品数量较多且对收入和利润有较大贡献,主营业务带来的净利润增长影响金额在6000万元至1亿元之间。
2023-12-03 17:06
【双鹭药业:长效粒细胞已开始销售,该产品已在国家医保目录】双鹭药业在互动平台表示,长效粒细胞规格:1.0ml:1.0mg;目前价格为658元/支,已经开始销售,该产品已在国家医保目录。
2023-10-19 18:52
双鹭药业:获得化学药品一类新药MBT-1608药物临床试验批准通知书
2023-10-19 18:46
【双鹭药业近日获得化学药品一类新药MBT-1608的药物临床试验批准通知书】双鹭药业近日获得化学药品一类新药MBT-1608的药物临床试验批准通知书。
2023-10-16 17:58
双鹭药业:公司在研项目GLP-1受体激动剂(日制剂)目前已完成三期所有入组受试者的随访,正处于临床数据整理阶段,初步结果显示我司研发产品和原研药诺和力®疗效基本一致,安全性无差异。该产品未单独进行减肥临床研究,但在Ⅲ期临床研究中将基线和24周后的体重变化作为次要疗效指标观察
2023-10-15 15:28
【双鹭药业:减肥药周制剂预计明年上半年完成临床研究】10月15日电,双鹭药业在互动平台表示,减肥药周制剂目前正在Ⅲ期临床入组随访中,预计11月份能完成所有受试者的入组工作,明年上半年完成临床研究。该产品主要用于二型糖尿病治疗,次要疗效指标为减轻体重。
2023-09-22 16:10
双鹭药业:获得聚乙二醇化人粒细胞刺激因子注射液药品注册证书
2023-06-30 17:34
【双鹭药业:“长效立生素项目”研发投入截止目前超5000万元】双鹭药业在投资者互动平台表示,该项目研发投入截止到目前超过5000万元。
2023-06-19 18:49
双鹭药业:获得注射用盐酸吉西他滨药品注册证书
2023-04-10 17:43
双鹭药业:获得注射用伏立康唑药品注册证书
2023-03-22 18:05
双鹭药业:获得达格列净片药品注册证书
2023-03-02 16:51
【双鹭药业:公司奥司他韦已获批,预计很快就会上市销售】双鹭药业在投资者互动平台表示,公司奥司他韦已获批,预计很快就会上市销售。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 揭秘连板股缺位(断板)战法:精准捕捉市场断层,实现高效接力
- 解读股市调整节奏:顺势与逆势的智慧
- 掌握抄底秘诀,捕捉股市机遇
- 散户股市生存法则:智慧布局,规避套牢
- 股市智慧:精准止损与高效止盈的艺术
- 股市智胜:老股民三大实战技巧深度剖析
- K线、均线、成交量:全面解析低价圈判断方法
- 期货交易全攻略:从零开始掌握买卖技巧
- 识破股市迷雾:真突破与假突破的较量
- 融资融券的风险与防范:深度解析爆仓现象
- 精准捕捉满仓时机:市场情绪与策略并重的艺术
- 揭秘主力吸筹手法:如何伺机买入?
- 股市稳健航行:构建良好心态与恪守炒股纪律的艺术
- 掌握止损技巧,稳健炒股之道
- 短线交易入门:精准把握市场脉搏,揭秘高效盈利策略
- 捕抓庄家介入黑马股:深度解析与实战技巧
- RSI指标的深度剖析:实战应用中的优势与缺陷
- 掌握T+0分时买卖绝技,炒股化“险”为“益”
- 掌握30日均线实战技巧,洞悉股市趋势
- 深入解析庄家吸筹策略与手法
当前版本:V3.0

 VIP复盘网
VIP复盘网
